
| A. | 元素的原子序数等于核电荷数 | |
| B. | 元素原子的质子数等于核外电子数 | |
| C. | 元素所在周期序数等于该元素原子的最外层电子数 | |
| D. | 元素所在周期序数等于该元素原子的电子层数 |
分析 A、在原子中质子数=核电荷数=核电荷数;
B、原子呈电中性,质子数等于核外电子数;
C、周期表中,主族元素的族序数等于最外层电子数;
D、周期表中,原子核外电子层数等于周期数;
解答 解:A、在原子中质子数=核电荷数=核电荷数,所以元素的原子序数等于核电荷数,故A正确;
B、原子呈电中性,质子数等于核外电子数,故B正确;
C、周期表中,主族元素的族序数等于最外层电子数,则周期序数等于该元素原子核外电子层数,故C错误;
D、周期表中,原子核外电子层数等于周期数,故D正确;
故选C.
点评 本题综合考查元素周期表与周期律知识,为高频考点和常见题型,注意把握元素周期表的构成以及原子的核外电子排布特点,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 1:1 | B. | 2:3 | C. | 1:2 | D. | 2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | C3H4和 H2 | B. | C3H8和 CO | C. | CH4和 C3H4 | D. | C3H6和 CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 天然橡胶分子中含有碳碳双键,能发生加成反应 | |
| B. | 硫化橡胶遇汽油能发生溶胀现象 | |
| C. | 聚硫橡胶具有良好的耐严寒,耐高温性能 | |
| D. | 合成橡胶是以石油、天然气为原料,以二烯烃和烯烃为单体聚合而成分高分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某学生用0.100 0mol•L-1盐酸标准溶液测定某烧碱样品的纯度(杂质不与盐酸反应).实验步骤如下:
某学生用0.100 0mol•L-1盐酸标准溶液测定某烧碱样品的纯度(杂质不与盐酸反应).实验步骤如下:| 滴定次数 | 待测液体积 | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 20.00 | 0.20 | 20.38 |
| 第二次 | 20.00 | 4.00 | 24.20 |
| 第三次 | 20.00 | 2.38 | a |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 离子 | 开始沉淀pH | 完全沉淀pH |
| Fe3+ | 2.1 | 3.2 |
| Al3+ | 4.1 | 5.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHCO3═Na++H++CO32- | B. | H2SO4═2H++SO42- | ||
| C. | Ba(OH)2═Ba2++2OH- | D. | Al2(SO4)3═3SO42-+2Al3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

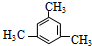 .
.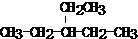 ,其名称为3-乙基戊烷.
,其名称为3-乙基戊烷.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com