
| 物质 | 组成和结构信息 |
| a | 含有A的二元离子化合物 |
| b | 含有共价键的二元离子化合物,且原子数之比为1:1 |
| c | 化学组成为ADF |
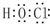 .
. 分析 A、B、D、E、F为短周期元素,非金属元素A最外层电子数与其周期数相同,则A为H元素;E+与D2-具有相同的电子数,则E处于IA族,D处于ⅥA族,则E为Na、D为O元素;B在D中充分燃烧生成其最高价化合物BD2,B的最高正化合价为+4,B的最外层电子数是其所在周期数的2倍,则B处于第二周期,故B为碳元素;A在F中燃烧,产物溶于水得到种强酸,则F为Cl.
(1)实验室利用二氧化锰与浓盐酸在加热条件下制备氯气;
(2)C、O、Na组成的一种盐,Na的质量分数为43%,则该盐为碳酸钠;
(3)a由两种元素组成且含有氢元素的离子化合物,这几种元素只有Na能与H形成离子化合物,故a为NaH;b由两种元素组成含有共价键的离子化合物,且原子数之比为1:1,则b为Na2O2和Na2C2;c的化学组成为HClO.
解答 解:A、B、D、E、F为短周期元素,非金属元素A最外层电子数与其周期数相同,则A为H元素;E+与D2-具有相同的电子数,则E处于IA族,D处于ⅥA族,则E为Na、D为O元素;B在D中充分燃烧生成其最高价化合物BD2,B的最高正化合价为+4,B的最外层电子数是其所在周期数的2倍,则B处于第二周期,故B为碳元素;A在F中燃烧,产物溶于水得到种强酸,则F为Cl.
(1)A为H元素,处于周期表中第一周期IA族;实验室利用二氧化锰与浓盐酸在加热条件下制备氯气,离子方程式为:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O,
故答案为:第一周期IA族;MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;
(2)C、O、Na组成的一种盐,Na的质量分数为43%,则该盐为碳酸钠,俗名为纯碱;故答案为:纯碱;
(3)a由两种元素组成且含有氢元素的离子化合物,这几种元素只有Na能与H形成离子化合物,故a为NaH;b由两种元素组成含有共价键的离子化合物,且原子数之比为1:1,则b为Na2O2和Na2C2;c的化学组成为HClO,电子式为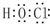 ,故答案为:NaH;Na2O2和Na2C2;
,故答案为:NaH;Na2O2和Na2C2;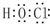 .
.
点评 本题考查元素化合物推断,题目涉及的知识点较多,侧重于考查学生对所学知识点综合应用能力,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 10℃20 mL 3 mol/L的盐酸 | B. | 10℃40 mL 2 mol/L的盐酸 | ||
| C. | 20℃20 mL 2 mol/L的盐酸 | D. | 20℃10 mL 4 mol/L的盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2Cl2+Cl2$\stackrel{光照}{→}$CHCl3+HCl | |
| B. | CH2═CH2+HBr→CH3CH2Br | |
| C. | 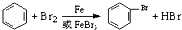 | |
| D. | 2CH3COOH+Na2CO3→2CH3COONa+CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4HCO3 $\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O+CO2↑ | |
| B. | C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O | |
| C. | 3Cl2+6NaOH═5NaCl+NaClO3+3H2O | |
| D. | 2HCl+CaCO3═CaCl2+CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
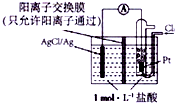
| A. | 正极为Pt电极,电极反应为2Ag++Cl2+2e-═2AgCl↓ | |
| B. | 放电时,交换膜两侧溶液中盐酸浓度不变 | |
| C. | 若用NaCl溶液代替盐酸,则电池总反应随之改变 | |
| D. | 当电路中转移0.01mole-时,交换膜左侧溶液中约减少0.02mol离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
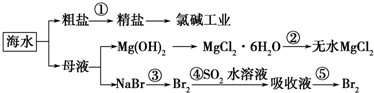
| A. | 除去粗盐中杂质(Mg2+、SO42-、Ca2+),加入的药品顺序为:NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸 | |
| B. | 在过程②中将MgCl2•6H2O灼烧即可制得无水MgCl2 | |
| C. | 从能量转换角度来看,氯碱工业中的电解饱和食盐水是一个将化学能转化为电能的过程 | |
| D. | 从第③步到第⑤步的目的是为了浓缩 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AlCl3溶液:Na+、K+、SO42-、AlO2- | |
| B. | KW/c(OH-)=0.1mol/L的溶液:Na+、Mg2+、NO3-、S2- | |
| C. | 无色溶液:Na+、Ca2+、I-、NO3- | |
| D. | 能使甲基橙呈黄色的溶液:H+、ClO-、Fe2+、Ag+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在标准状况下,2.24L 苯中含有 0.6NA个碳原子 | |
| B. | 1 L PH=l的硫酸溶液中含有0.2NA个氢离子 | |
| C. | 1 L 1 mol•L-1的 FeC13溶液中,含有铁离子的数目为NA | |
| D. | t℃时,1 L pH=6的纯水中,含有10-6NA个OH- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com