
【题目】下面是混合物分离的实验,请回答有关问题
实验:通过蒸馏的方法除去自来水中含有的氯离子等杂质制取纯净水,如图所示
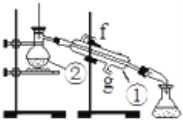
(1)写出下列仪器的名称:①________②________。
(2)若利用以上装置分离酒精和四氯化碳两种溶液的混合物,还缺少的仪器是________,图中装置中进水口是________。(填“f”或“g”)
(3)仪器①中常加入碎瓷片,这样做的目的是________。
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案科目:高中化学 来源: 题型:
【题目】化学在能源开发与利用中起着十分关键的作用。
(1)蕴藏在海底的“可燃冰”是高压下形成的外观象冰的甲烷水合物固体。甲烷气体燃烧和水汽化的热化学方程式分别为:
CH4(g)+ 2O2(g)═ CO2(g)+ 2H2O(g)△H=﹣802.3kJmol﹣1,
H2O(l)═ H2O(g)△H= +44kJmol﹣1;
则356g“可燃冰”(分子式为CH49H2O)释放的甲烷气体完全燃烧生成液态水,放出的热量为________。
(2)0.3mol的气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5kJ热量,其热化学方程式为________。
(3)家用液化气中主要成分之一是丁烷(C4H10)。常温常压时,当1g丁烷完全燃烧并生成CO2和液态水时,放出热量50kJ。试写出该状态下表示丁烷燃烧热的热化学方程式________。
(4)联合国气候变化大会于2009年12月7~18日在哥本哈根召开。中国政府承诺到2020年,单位GDP二氧化碳排放比2005年下降40%~45%。
①有效“减碳”的手段之一是节能。下列制氢方法最节能的是________(填字母序号)。
A.电解水制氢:2H2O ![]() 2H2↑+O2↑
2H2↑+O2↑
B.高温使水分解制氢:2H2O ![]() 2H2↑+O2↑
2H2↑+O2↑
C.太阳光催化分解水制氢:2H2O ![]() 2H2↑+O2↑
2H2↑+O2↑
D.天然气制氢:CH4+H2O ![]() CO+3H2
CO+3H2
②用CO2和氢气合成CH3OCH3(甲醚)是解决 能源危机的研究方向之一。
已知:CO(g)+2H2(g)![]() CH3OH(g)△H=﹣90.7kJmol﹣1
CH3OH(g)△H=﹣90.7kJmol﹣1
2CH3OH(g)![]() CH3OCH3(g)+H2O(g)△H=﹣23.5kJmol﹣1
CH3OCH3(g)+H2O(g)△H=﹣23.5kJmol﹣1
CO(g)+H2O(g)![]() CO2(g)+H2(g)△H=﹣41.2kJmol﹣1
CO2(g)+H2(g)△H=﹣41.2kJmol﹣1
则CO2和氢气合成CH3OCH3(g)和水蒸气的热化学方程式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图所示,A处通入干燥Cl2,关闭B阀时,C处的红色布条看不到明显现象,打开B阀后,C处红色布条逐渐褪色,则D瓶中装的是
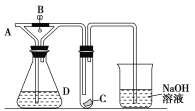
A.浓H2SO4 B.浓盐酸 C.NaOH溶液 D.饱和NaCl溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在氧化还原反应3S+6KOH=K2SO3+2K2S+3H2O中,氧化剂和还原剂的物质的量之比为( )
A.1:2
B.2:1
C.1:1
D.3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钼(Mo)是一种过渡金属元素,它具有强度高、熔点高、耐腐蚀等优点,被广泛应用于钢铁、石油、化工、电气等领域。钼酸钠晶体(Na2MoO4·2H2O)是一种新型水处理剂。某化学兴趣小组利用废钼催化剂(主要成分为MoS2,含少量Cu2S,FeS2)回收Mo并制备钼酸钠晶体,其主要流程图如图所示:
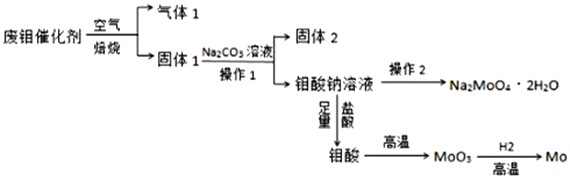
回答下列问题:
(1)可以提高焙烧效率的措施有____________________________________(填一条即可),MoS2中的钼元素在空气中焙烧,很容易被氧化成MoO3,若反应中生成0.1molMoO3,反应中转移电子的数目为____________;
(2)往固体1中加碳酸钠溶液发生反应的化学方程式为______________________________;
(3)操作2为______________________________;
(4)制备钼酸钠晶体还可用通过向精制的MoS2中直接加入次氯酸钠溶液与氢氧化钠溶液进行氧化的方法,若氧化过程中,还有硫酸钠生成,则反应的离子方程式为______________;
(5)已知钼酸钠溶液中c(MoO42-)=0.40molL-1,由钼酸钠溶液制备钼酸钠晶体时,需加入Ba(OH)2固体以除去CO32-,当BaMoO4开始沉淀时,CO32-的浓度为__________________;[已知:Ksp(BaCO3)=2.6×10-9,Ksp(BaMoO4)=4.0×10-8,忽略溶液的体积变化]
(6)锂和二硫化钼形成的二次电池的总反应为:xLi+nMoS2![]() Lix(MoS2)n[Lix(MoS2)n附着在电极上],则电池充电时阳极的电极反应式为__________________________________。
Lix(MoS2)n[Lix(MoS2)n附着在电极上],则电池充电时阳极的电极反应式为__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电炉加热时用纯O2氧化管内样品,根据产物的质量确定有机物的组成。如图1装置是用燃烧法确定有机物分子式常用的装置。
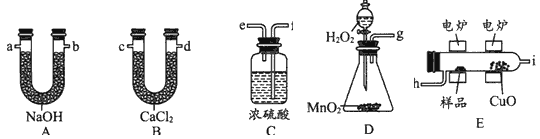
(1)D装置中MnO2的作用是_________________。
(2)燃烧管中CuO的作用是_____________________。
(3)若实验中所取样品只含C、H、O三种元素中的两种或三种,准确称取0.92 g样品,经充分反应后,A管质量增加1.76 g,B管质量增加1.08 g,则该样品的实验式为__________________。
(4)用质谱仪测定其相对分子质量,得如图2所示的质谱图,则该有机物的相对分子质量为___。
(5)该物质的核磁共振氢谱如图二所示,则其结构简式为_____________。
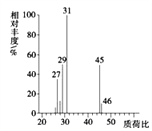
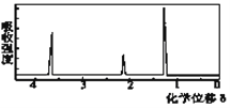
图2 图3
查看答案和解析>>
科目:高中化学 来源: 题型:
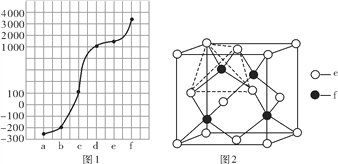
【题目】a、b、c、d、e、f分别是H、C、N、Na、Si、Cu六种元素中的其中一种,已知:图1表示的是六种元素单质的熔点高低顺序,其中c、d均是热和电的良导体,f形成的某种单质硬度最大。
回答下列问题:
(1)a、b、f三种元素的电负性从小到大的顺序为________(用元素符号表示)。
(2)元素b的单质的一个分子中含有________个σ键和_________个π键。
(3)元素c的单质的晶体堆积方式类型是_______________________;若c单质分别与氟气和氯气形成化合物甲和乙,则甲的晶格能________乙的晶格能(填“>”“<”或“=”)。
(4)元素d的基态原子的价电子排布式为__________________。
(5)元素e和f可形成化合物丙(丙的晶胞结构如图2所示),则丙的化学式为_________;丙的晶体类型为_______________,在丙中,每个e原子周围最近的e原子数目为_____,若晶胞的边长为a pm,则丙的密度为____________g·cm-3(用NA表示阿伏加德罗常数的值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室模拟工业漂白液(有效成分为NaClO)脱除废水中氨氮(NH3)的流程如下:
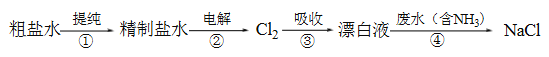
下列分析正确的是
A. ①中采用蒸馏的方法精制粗盐水
B. ②中阳极的主要电极反应:4OH- - 4e- = 2H2O + O2↑
C. ③中制备漂白液的反应:Cl2 + OH- = Cl- + HClO
D. ②、③、④中均发生了氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在溶液中能大量共存的是
A. Al3+、Na+、HCO3-、[Al(OH)4]-
B. Ca2+、HCO3-、Cl-、K+
C. Fe3+、H+、SO42-、S2-
D. Fe2+、NO3-、Na+、H+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com