
【题目】能被酸性高锰酸钾溶液氧化的物质是
A. 乙烷 B. 乙醇 C. 苯 D. 乙酸
 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:
【题目】将金属钠放入盛有下列溶液的小烧杯中,既有气体产生,又有白色沉淀产生的是( )
A.NaHCO3溶液B.MgSO4溶液C.FeCl3溶液D.HCl溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于2X(g)![]() Y(g)的体系,在压强一定时,平衡体系中Y的质量分数w(Y)随温度的变化情况如图所示(实线上的任何一点为对应温度下的平衡状态)。
Y(g)的体系,在压强一定时,平衡体系中Y的质量分数w(Y)随温度的变化情况如图所示(实线上的任何一点为对应温度下的平衡状态)。

(1)该反应的正反应方向是一个________反应(“吸热”或“放热”)。
(2)A、B、C、D、E各状态中,v正<v逆的点是____________。
(3)维持t1不变,E→A所需时间为x,维持t2不变,D→C所需时间为y,则x ______ y(填“<”、“>”或“=”)。
(4)欲使E状态从水平方向到C状态后,再沿平衡曲线到达A状态,从理论上来讲,可选用的条件是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知A~H均为中学化学常见的物质,转化关系如下图。其中A、C均为金属单质,C与水反应生成D和最轻的气体,D、F、G、H的焰色反应均为黄色,E为两性化合物。

(1)写出C与水反应的离子方程式_____________________________________,假设温度不变,该反应会使水的电离程度________(填写“变大”“变小”“不变”)
(2)B的水溶液呈_________性,用离子方程式解释原因______________
(3)将A~H中易溶于水的化合物溶于水,会抑制水的电离的是____________(填序号)
(4)常温下,pH均为10的D、F溶液中,水电离出的c(OH-)之比为___________________向D的稀溶液中通入CO2至溶液呈中性,所得溶液中离子物质的量浓度由大到小的顺序为:_______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学中常用图像直观地描述化学反应的进程或结果,下列图像描述正确的是

A. 图①可以表示对某化学平衡体系改变温度后反应速率随时间的变化
B. 图②表示压强对可逆反应2A(g)+2B(g)![]() 3C(g)+D(g)的影响,且甲的压强大
3C(g)+D(g)的影响,且甲的压强大
C. 图③表示向Al2(SO4)3和MgSO4的混合液中滴加NaOH溶液,生成沉淀的量与滴入NaOH溶液体积的关系
D. 图④表示在2 L的密闭容器中发生合成氨反应时N2的物质的量随时间的变化曲线,0~10 min内该反应的平均速率v(H2)=0.045 mol·L-1·min-1,从11 min起其他条件不变,压缩容器的体积为1 L,则n(N2)的变化曲线为d
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述错误的是( )
A.乙烯和苯都能使溴水褪色,褪色的原因相同
B.乙醇室温下在水中的溶解度大于苯酚
C.煤油可由石油分馏获得,可用作燃料和保存少量金属钠
D.利用过滤法不能将苯与三溴苯酚的混合物分离
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(14分)按要求完成下列填空
Ⅰ.已知:①2C3H8(g)+7O2(g)=6CO(g)+8H2O(l) ΔH=-2741.8kJ/mol
②2CO(g)+O2(g)=2CO2(g) ΔH="-566" kJ/mol
(1)反应C3H8(g)+5O2(g)=3CO2(g)+4H2O(l)的ΔH= ;
(2)C3H8在不足量的氧气里燃烧,生成CO和CO2以及气态水,将所有的产物通入一个固定体积的密闭容器中,在一定条件下发生如下可逆反应:CO(g)+ H2O(g)![]() CO2(g)+ H2(g) ΔH>0
CO2(g)+ H2(g) ΔH>0
①下列事实能说明该反应达到平衡的是 ;
a.体系中的压强不发生变化
b.υ正(H2)=υ逆(CO)
c.混合气体的平均相对分子质量不发生变化
d.CO2的浓度不再发生变化
②在某温度下,反应物的起始浓度分别为:c(CO)=" 1" mol·L-1, c(H2O)="2.4" mol·L-1; 达到平衡后,CO的转化率为60%,该反应在此温度下的平衡常数是 ;
(3)熔融碳酸盐燃料电池的电解质为Li2CO3和 Na2CO3的混合物,燃料为CO,在工作过程中,电解质熔融液的组成、浓度都不变,写出负极发生的电极反应式 。
Ⅱ.氮化硅(Si3N4)是一种新型陶瓷材料,它可用石英与焦炭在高温的氮气流中反应制得:
SiO2 + C + N2![]() Si3N4 + CO 根据题意完成下列各题:
Si3N4 + CO 根据题意完成下列各题:
(1)配平上述化学反应方程式。 SiO2 + C + N2![]() Si3N4 + CO
Si3N4 + CO
(2)为了保证石英和焦炭尽可能的转化,氮气要适当过量。某次反应用了30mol氮气,反应生成了5mol一氧化碳,则此时混合气体的平均摩尔质量是 。
(3)氮化硅陶瓷的机械强度高,硬度接近于刚玉(A12O3),热稳定性好,化学性质稳定。以下用途正确的是 。
A.可以在冶金工业上制成坩埚、铝电解槽衬里等设备 |
B.在电子工业上制成耐高温的电的良导体 |
C.研发氮化硅的全陶发动机替代同类型金属发动机 |
D.氮化硅陶瓷的开发受到资源的限制,没有发展前途 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2的含量是衡量大气污染的一个重要指标,工业上常采用催化还原法或吸收法处理SO2。利用催化还原SO2不仅可消除SO2污染,而且可得到有经济价值的单质S。
(1)在复合组分催化剂作用下,CH4可使SO2转化为S,同时生成CO2和H2O。
己知CH4和S的燃烧热(△H)分别为-890.3 kJ /mol和-297.2 kJ /mol,则CH4和SO2反应的热化学方程式为 _________________________________________________。
(2)用H2还原SO2生成S的反应分两步完成,如图1所示,该过程中相关物质的物质的量浓度随时间的变化关系如图2所示:
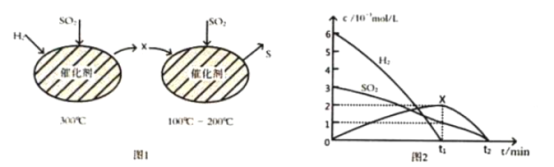
①分析可知X为________(写化学式), 0~t1时间段的温度为_____, 0~t1时间段用SO2表示的化学反应速率为 ___________________________。
②总反应的化学方程式为__________________________________________________________。
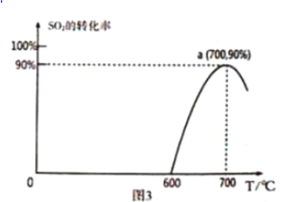
(3)焦炭催化还原SO2生成S2,化学方程式为:2C(s)+2SO2(g)![]() S2(g)+2CO2(g),恒容容器中,1 mol/LSO2与足量的焦炭反应,SO2的转化率随温度的变化如图3所示。
S2(g)+2CO2(g),恒容容器中,1 mol/LSO2与足量的焦炭反应,SO2的转化率随温度的变化如图3所示。
①该反应的△H _________________________ 0 (填“>”或“<”)
②计算700℃该反应的平衡常数为____________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求写出下列化学方程式或离子方程式:
(1)硫酸酸化的高锰酸钾与草酸反应的化学方程式:_____________________________。
(2)硫代硫酸钠与稀硫酸反应的化学方程式:____________________________________。
(3)硫酸酸化的碘化钾溶液与氧气反应的离子方程式:________________________。
(4)K2Cr2O7的溶液中K2Cr2O7与K2CrO4转化的离子方程式:____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com