
1 mol过氧化钠与2 mol碳酸氢钠固体混合后,在密闭容器中加热充分反应,排出气体物质后冷却,残留的固体物质是( )
A.Na2CO3 B.Na2O2、Na2CO3
C.NaOH、Na2CO3 D.Na2O2、NaOH、Na2CO3
A
【解析】
试题分析:Na2O2与NaHCO3的混合物受热分解时,首先是NaHCO3分解,即
2NaHCO3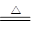 Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
2mol 1mol 1mol 1mol
产生的CO2与H2O均可与Na2O2反应,由于Na2O2与H2O反应生成NaOH,而NaOH又可与CO2反应生成H2O,故可以认为是CO2先与Na2O2反应,CO2耗尽后H2O才开始反应。而根据2Na2O2+2CO2===2Na2CO3+O2可知,生成的1 mol CO2恰好与1 mol Na2O2完全反应生成Na2CO3,H2O不会再与Na2O2反应,故最终固体产物只有Na2CO3,答案选A。
考点:考查过氧化钠和碳酸氢钠混合加热的有关计算
点评:该题是高考中的常见题型,属于难度较大的计算题。该题的关键是准确判断出CO2和水蒸气与过氧化钠反应的先后顺序,然后即可得出正确的结论。该题有利于培养学生严谨的逻辑思维能力,提高学生的学习效率。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2013-2014学年高考化学三轮复习排查 专题10金属元素及其化合物练习卷(解析版) 题型:选择题
1 mol过氧化钠与2 mol碳酸氢钠固体混合后,在密闭容器中加热充分反应,排出气体物质后冷却,残留的固体物质是???? ( )。
A.Na2CO3???????????????? B.Na2O2、Na2CO3
C.NaOH、Na2CO3?????????? D.Na2O2、NaOH、Na2CO3
查看答案和解析>>
科目:高中化学 来源:2010年广州市花都区高三上学期调研考试(理综)化学部分 题型:选择题
下列关于NA说法正确的是 ( )
A.0.1 mol 过氧化钠与足量水反应生成的O2分子数为0.1 NA
B、100 mL 2.0 mol•L-1的盐酸与醋酸溶液中氢离子数均为0.2NA
C.室温下,28.0g乙烯和丙烯混合气体中含有的碳原子数为2NA
D.标准状况下,11.2L臭氧中含有的氧原子数目为3NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com