
| A. | 60g丙醇含有的共价键数目为10NA | |
| B. | 常温常压下,4.4gCO2与N2O混合气体中含有的原子数为0.3NA | |
| C. | 在过氧化钠与水的反应中,每生成0.1mol氧气,转移电子的数目为0.4NA | |
| D. | 80ml10mol/L盐酸与足量MnO2加热反应,产生Cl2的分子数为0.2NA |
分析 A、求出丙醇的物质的量,然后根据丙醇中含11条共价键来分析;
B、CO2与N2O的摩尔质量均为44g/mol,且均含3个原子;
C、过氧化钠和水反应生成氧气时,氧元素由-1价变为0价;
D、二氧化锰只能与浓盐酸反应,和稀盐酸不反应.
解答 解:A、60g丙醇的物质的量为1mol,而丙醇中含11条共价键,故1mol丙醇中含11NA条共价键,故A错误;
B、CO2与N2O的摩尔质量均为44g/mol,故4.4g混合物的物质的量为0.1mol,且两者均含3个原子,故0.1mol混合物中含0.3NA个原子,故B正确;
C、过氧化钠和水反应生成氧气时,氧元素由-1价变为0价,故生成0.1mol氧气时转移0.2NA个电子,故C错误;
D、二氧化锰只能与浓盐酸反应,和稀盐酸不反应,故浓盐酸不能反应完全,则生成的氯气分子个数小于0.2NA个,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.


 通城学典默写能手系列答案
通城学典默写能手系列答案科目:高中化学 来源: 题型:选择题
| A. | 用K2FeO4代替Cl2处理饮用水,既有杀菌消毒作用,又有净水作用 | |
| B. | 古有“青蒿一握,以水二升渍,绞取汁”,今用乙醚从黄花蒿中提取青蒿素是利用氧化还原反应原理 | |
| C. | 面粉中禁止添加CaO2、过氧化苯甲酰等增白剂,CaO2属于碱性氧化物合物,也属于离子化合物,其阴阳离子冷数比为2:l,过氧化苯甲酞属于有机物 | |
| D. | 二氧化硫有毒,产禁将其添加到任何食品和饮料中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 简单的离子半径:W>Z>Y>X | |
| B. | 五种元素中只有X存在同素异形体 | |
| C. | W和M形成的化合物是离子化合物 | |
| D. | 工业上采用电解W和Z形成的化合物制备W单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| R | T | |
| X | Y | Z |
| A. | R位于元素周期表中第二周期第VA族 | |
| B. | R能分别与X、Z形成共价化合物 | |
| C. | 原子半径大小顺序为X>T>Y | |
| D. | Z元素的最高价氧化物对应的水化的化学式为HZO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
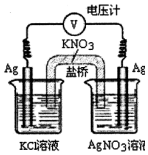 一定条件下,实验室利用如图所示装置,通过测电压求算Kkp(AgCl).工作一段时间后,两电极质量均增大.下列说法正确的是( )
一定条件下,实验室利用如图所示装置,通过测电压求算Kkp(AgCl).工作一段时间后,两电极质量均增大.下列说法正确的是( )| A. | 右池中的银电极作正极 | B. | 总反应为Ag++Cl-═AgCl | ||
| C. | 正极反应为Ag-e-═Ag+ | D. | 盐桥中的NO3-向右池方向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 编号 | ① | ② | ③ | ④ |
| 装置 | 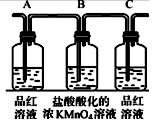 |  |  | 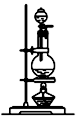 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a>b | B. | a<b | C. | a=b | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com