
| A、-57.3mol/L |
| B、-57.3kJ/mol |
| C、+57.3J/mol |
| D、-57.3J/mol |
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、使红色布条褪色(HCl) |
| B、氯水呈黄绿色(Cl2) |
| C、将NaHCO3固体加入新制氯水,有无色气泡(H+) |
| D、滴加AgNO3溶液生成白色沉淀(Cl-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
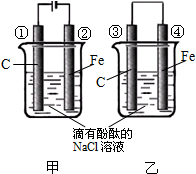 化学能和电能的相互转化,是能量转化的重要方式之一,如图所示两个实验装置是实现化学能和电能相互转化的装置.
化学能和电能的相互转化,是能量转化的重要方式之一,如图所示两个实验装置是实现化学能和电能相互转化的装置.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、150mL 1mol?L-1氯化钠溶液 |
| B、75mL 1.5 mol?L-1氯化钙溶液 |
| C、150mL 3 mol?L-1氯化钾溶液 |
| D、75mL 1 mol?L-1氯化铁溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2SO2(g)+O2(g)?2SO3(g)为放热反应,则SO2的能量一定高于SO3的能量 |
| B、已知C(石墨,s)═C(金刚石,s)△H>0,则金刚石比石墨稳定 |
| C、H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ/mol,则任何中和反应的中和热为-57.3kJ/mol |
| D、已知2C(s)+2O2(g)═2CO2(g)△H1,2C(s)+O2(g)═2CO(g)△H2,则△H1<△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NH3?H2O+HCl=NH4Cl+H2O | ||||
| B、Cl2+H2O=HCl+HClO | ||||
| C、Cl2+2KI=2KCl+I2 | ||||
D、MnO2+4HCl(浓)
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2 L CO和2 L O2 |
| B、同温同压下,2LO2和N2与NO的混合气体2L |
| C、0.2 mol H2和4.48 L HCl |
| D、标准状况下2 mol CO2和44.8 L水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com