
| A、9和12 | B、1和11 |
| C、6和17 | D、3和8 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe-2e-═Fe2+ |
| B、Fe-3e-═Fe3+ |
| C、O2+2H2O+4e-═OH- |
| D、2H++2e-═H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、各物质的量浓度之比为c(A):c(B):c(C)═2:3:3 | ||
B、平衡混合物体积是反应开始前的
| ||
| C、平衡混合物中各物质的量浓度相等 | ||
| D、单位时间内,若消耗了a mol A物质,则同时也消耗了1.5a mol C物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、只用溴水一种试剂鉴别苯、己烯、乙醇、四氯化碳 |
| B、用KMnO4酸性溶液鉴别CH3CH=CHCH2OH和CH3CH2CH2CHO |
| C、用核磁共振氢谱鉴别1-溴丙烷和2-溴丙烷 |
| D、用银氨溶液或NaHCO3溶液鉴别甲酸甲酯和乙酸两种液体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硫酸和氢氧化钠反应属于放热反应 |
| B、一定量的燃料完全燃烧放出的热量比不完全燃烧放出的热量大 |
| C、放热反应的逆反应一定是吸热反应 |
| D、选择燃料只要考虑燃料热值的大小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙烯发生加聚反应制得聚乙烯高分子材料 |
| B、用甲烷与氯气制备一氯甲烷 |
| C、用苯和液溴为原料制取溴苯 |
| D、用石灰石和稀盐酸反应制得二氧化碳 |
查看答案和解析>>
科目:高中化学 来源: 题型:
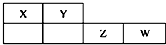 X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如下图所示.若Y原子的最外层电子数是次外层电子数的2倍,下列说法中正确的是( )
X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如下图所示.若Y原子的最外层电子数是次外层电子数的2倍,下列说法中正确的是( )| A、氢化物稳定性:X>Y |
| B、最高价氧化物对应的水化物的酸性:W>Y |
| C、4种元素的单质中,W单质的熔、沸点最高 |
| D、干燥的W单质具有漂白性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com