
将0.48 g Mg粉加入到500 mL 0.1 mol·L-1的硝酸中恰好完全反应,则还原产物可能是 ( )。
A.NO2 B.NO
C.N2O3 D.NH
科目:高中化学 来源: 题型:
对于常温下的0.1 mol·L-1的NH4Cl溶液,请填空:
(1)溶液的pH________7(填“>”、“<”或“=”)。
(2)各类离子,其浓度由大到小的排列顺序是______________。
(3)存在的电荷守恒关系为____________________________。
(4)c(NH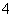 )+c(NH3·H2O)=________(填数字或离子浓度均可)。
)+c(NH3·H2O)=________(填数字或离子浓度均可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于如图所示装置的说法,正确的是( )
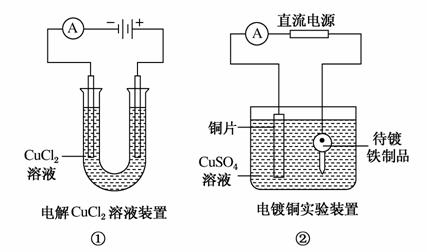

A.①装置中阴极处产生的气体能够使湿润KI淀粉试纸变蓝
B.②装置中待镀铁制品应与电源正极相连
C.③装置中电子由b极流向a极
D.④装置中的离子交换膜可以避免生成的Cl2与NaOH溶液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
镇痉药物C、化合物N以及高分子树脂(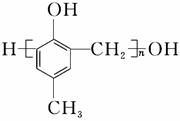 )的合成路线如下:
)的合成路线如下:
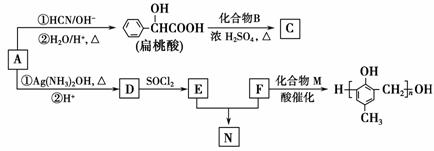
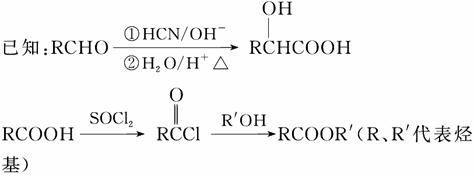
(1)A的含氧官能团的名称是________。
(2)A在催化剂作用下可与H2反应生成B。该反应的反应类型是________。
(3)酯类化合物C的分子式是C15H14O3,其结构简式是________________。
(4)A发生银镜反应的化学方程式是______________________________
_____________________________________________________________。
(5)扁桃酸(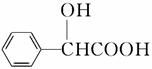 )有多种同分异构体。属于甲酸酯且含酚羟基的同分异构体共有________种,写出其中一种含亚甲基(—CH2—)的同分异构体的结构简式______________________。
)有多种同分异构体。属于甲酸酯且含酚羟基的同分异构体共有________种,写出其中一种含亚甲基(—CH2—)的同分异构体的结构简式______________________。
(6)F与M合成高分子树脂的化学方程式是___________________________
______________________________________________________________。
(7)N在NaOH溶液中发生水解反应的化学方程式是
___________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
据报道,化合物M对番茄灰霉菌有较好的抑菌活性,其合成路线如下图所示:
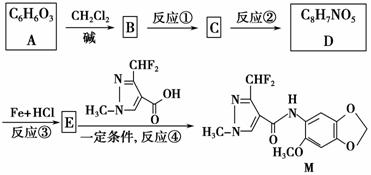

完成下列填空:
(1)写出反应类型:
反应③________;反应④________。
(2)写出结构简式:
A_____________________________________________________________;
E__________________________________________________________。
(3)写出反应②的化学方程式:_______________________________________
_________________________________________________________________。
(4)B的含苯环结构的同分异构体中,有一类能发生碱性水解,写出检验这类同分异构体中的官能团(酚羟基除外)的试剂及出现的现象:
试剂(酚酞除外):___________________________________________;
现象:_____________________________________________________。
(5)写出两种C的含苯环结构且只含4种不同化学环境氢原子的同分异构体的结构简式:
_________________________________________________________
_________________________________________________________。
(6)反应①、反应②的先后次序不能颠倒,请解释原因:_________________
____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在硫酸铁电化浸出黄铜矿精矿工艺中,有一主要反应:CuFeS2+4Fe3+===Cu2++5Fe2++2S,反应结束后,经处理获得单质硫x mol。下列说法正确的是 ( )。
A.反应中硫元素被氧化,所有铁元素均被还原
B.氧化剂是Fe3+,氧化产物是Cu2+
C.反应中转移电子的物质的量为x mol
D.反应结束后,测得溶液中三种金属离子的总物质的量为y mol,则原Fe3+的总物质的量为(y-x) mol
查看答案和解析>>
科目:高中化学 来源: 题型:
下列对各组物质性质的比较中,正确的是 ( )。
A.熔点:Li<Na<K
B.导电性:Ag>Cu>Al>Fe
C.密度:Na>Mg>Al
D.空间利用率:体心立方堆积<六方最密堆积<面心立方最密堆积
查看答案和解析>>
科目:高中化学 来源: 题型:
在100 ℃时,将0.100 mol N2O4气体充入1 L恒容抽空的密闭容器中,隔一定时间对该容器内物质的浓度进行分析得到如表数据:
| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| c(N2O4)/mol·L-1 | 0.100 | c1 | 0.050 | c3 | c4 |
| c(NO2)/mol·L-1 | 0.000 | 0.060 | c2 | 0.120 | 0.120 |
(1)该反应的平衡常数表达式为________;从表中分析:
c1________c2,c3________c4(填“>”、“<”或“=”)。
(2)在上述条件下,从反应开始直至达到化学平衡时,N2O4的平均反应速率为________mol·L-1·s-1。
(3)达平衡后下列条件的改变可使NO2气体浓度增大的是________(填字母序号)。
A.扩大容器的容积 B.再充入一定量的N2O4
C.分离出一定量的NO2 D.再充入一定量的He
(4)若在相同条件下,起始时只充入0.080 mol NO2气体,则达到平衡时NO2气体的转化率为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com