
分析 (1)根据电解质的定义分析,在水溶液里或熔融状态下能导电的化合物是电解质,包括酸、碱、盐、活泼金属氧化物和水;
(2)酸或酸式盐能电离出氢离子;
(3)电离出阴离子全是氢氧根离子的化合物为碱;根据物质的溶解性分析;
(4)根据物质的溶解性分析.
解答 解:(1)电解质包括酸、碱、盐、活泼金属氧化物和水,所以②NaCl③NaHSO4属于盐,⑤硫酸属于酸⑦CaCO3属于盐⑧BaSO4属于盐⑨Cu(OH)2 ⑩Fe(OH)3⑪NaOH⑫CaO属于氧化物都是电解质,
故答案为:②③⑤⑦⑧⑨⑩⑪⑫;
(2)③NaHSO4 ⑤H2SO4 能电离出氢离子;电离出的阳离子全部是氢离子的化合物为酸,故⑤为酸,故答案为:③⑤;⑤;
(3)⑨Cu(OH)2 ⑩Fe(OH)3⑪NaOH电离出的阴离子全是氢氧根离子属于碱,其中⑨Cu(OH)2 ⑩Fe(OH)3难溶于水,属于难溶性碱,故答案为:⑨⑩⑪;⑨⑩;
(4)碳酸钙、硫酸钡不溶于水,都属于难溶性盐,
故答案为:⑦⑧.
点评 本题考查学生酸碱盐概念及溶解性、电解质的判断,注意概念的整理和把握是关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | ①②④ | B. | ①③④ | C. | ②③④ | D. | ①②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaCl晶体、BaSO4 | B. | Na2SO4、酒精 | ||
| C. | 铜、二氧化硫 | D. | 熔融的KNO3、硫酸溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径由小到大的顺序:X<Y<Z<W | |
| B. | X氢化物的沸点高于Z氢化物的沸点 | |
| C. | 最高价氧化物对应水化物的酸性X大于Z | |
| D. | 室温下,0.1 mol/L W的气态氢化物的水溶液的pH>1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
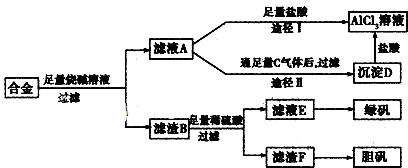

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 能量的发展发段为:柴草时期→化石能源时期→多能源结构时期 | |
| B. | 化石燃料种类:煤、石油、天然气,特点:蕴藏量有限,且不能再生 | |
| C. | 新能源特点:资源丰富,可以再生,没有污染 | |
| D. | 我国目前使用的主要能源是:化石燃料,它们的蕴藏量有限,而且不能再生,最终将会枯竭 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:9 | B. | 10:1 | C. | 9:1 | D. | 1:10 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com