
| A.钠原子和氯原子作用生成NaCl后,其结构的稳定性增强 |
| B.在氯化钠中,氯离子和钠离子靠静电作用结合 |
| C.任何离子键在形成的过程中必定有电子的得与失 |
| D.金属钠与氯气反应生成氯化钠后,体系能量降低 |
 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案科目:高中化学 来源:不详 题型:单选题
| A.①④⑥ | B.①②③④⑤ | C.①④ | D.①②③ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.NH4Cl NH3↑+HCl↑ NH3↑+HCl↑ |
B.NH3+CO2+H2O NH4HCO3 NH4HCO3 |
C.2NaOH+Cl2 NaCl+NaClO+H2O NaCl+NaClO+H2O |
D.2Na2O2+2CO2 2Na2CO3+O2 2Na2CO3+O2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| O—O键 数据 | O22- | O2- | O2 | O2+ |
| 键长/10-12m | 149 | 128 | 121 | 112 |
| 键能/kJ·mol-1 | X | Y | Z=494 | W=628 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.ⅠA族元素成键时不可能有杂化轨道 |
| B.杂化轨道既可能形成σ键,也可能形成π键 |
| C.孤对电子有可能参加杂化 |
| D.s轨道和p轨道杂化不可能有sp4出现 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.只有非金属原子间才能形成共价键 |
| B.共价化合物中不可能含有离子键 |
| C.单质中不可能含有离子键 |
| D.非金属单质中不一定含有共价键 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
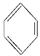 ;④CHCH;⑤NH3;⑥CH4
;④CHCH;⑤NH3;⑥CH4| A.①②③ | B.①⑤⑥ | C.②③④ | D.③⑤⑥ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com