
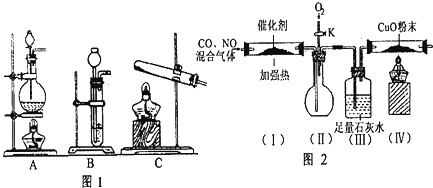
���� ��1����ͭмϡ����Ϊԭ����ȡ����ͭ��ͭ��ϡ���ᷴӦ��������ͭ��һ�����������ˮ��
��2��ѡ������ķ���װ�ø��ݷ�Ӧ���״̬�ͷ�Ӧ��������Ϸ�Ӧԭ��HCOOH$\frac{\underline{\;\;��\;\;}}{\;}$CO��+H2O���÷�ӦΪҺ�����װ�ã���Ũ����Ͷ������̼��ȿ���ȡ������
��3��ģ������β���������̣�װ�ã�I����CO��NO�������ͨ������������Ӧ��2CO+2NO$\frac{\underline{����}}{��}$2CO2+N2��ʵ��ǰ���ر�����K����ͨ�����ž�װ���еĿ�������ֹ��ȼ�������������������Ϸ�����ը��װ�ã�II���������������٣�װ�ã�III��������CO�Ƿ�ת��ΪCO2��װ�ã�������һ����̼������ͭ��Ӧ��һ����̼��һ�������ж������Է�ֹһ����̼��һ������й©�Ӷ���Ⱦ��������Ӧ��װ�ã�������β������װ�ã�
�ٿ�ȼ�������ڵ�ȼǰ����Ҫ�鴿����ֹ������ը��
��CO2�������ʯ��ˮ����ǣ���һ����̼���ܣ�
��� �⣺��1��ͭ���л�ԭ�ԣ�������������ԣ�ͭ��ϡ���ᷢ��������ԭ��Ӧ����������ͭ��һ�����������ˮ����Ӧ�Ļ�ѧ����ʽΪ3Cu+8HNO3��ϡ��=3Cu��NO3��2+2NO��+4H2O����Ӧ�����ӷ���ʽΪ��3Cu+8H++2NO3-=3Cu2++2NO��+4H2O��
�ʴ�Ϊ��3Cu+8H++2NO3-=3Cu2++2NO��+4H2O��
��2�����ݷ�Ӧ����ʽHCOOH$\frac{\underline{\;\;��\;\;}}{\;}$CO��+H2O��֪���÷�ӦΪҺ�塢����װ�ã�Ӧ��ѡ��װ��A����װ�û�����Ũ����Ͷ������̼���MnO2+4HCl��Ũ�� $\frac{\underline{\;\;��\;\;}}{\;}$MnCl2+Cl2��+2H2O����ȡCl2��
�ʴ�Ϊ��A��Cl2��
��3����ʵ��ǰ���ر�����K����ͨ�����ž�װ���еĿ�������ֹ��ȼ�������������������Ϸ�����ը��
�ʴ�Ϊ����ֹCO�������ϼ��ȱ�ը��
��CO2�������ʯ��ˮ����ǣ���һ����̼���ܣ�����װ�ã�III������Ҫ�����Ǽ���CO�Ƿ�ת��ΪCO2��
�ʴ�Ϊ������CO�Ƿ�ת��ΪCO2��
���� ���⿼��������ʵ�鷽���������ǽ������������ʵ�̽������Ŀ�Ѷ��еȣ���ȷʵ��ԭ������ѧʵ�������������Ϊ���ؼ��������ֿ�����ѧ���ķ�����������������ѧʵ��������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������̼ͨ�����������������Һ��CO2+2OH-�TCO32-+H2O | |
| B�� | ̼��������ᷴӦ��CO32-+2H+�TH2O+CO2�� | |
| C�� | ���������Ʒ�����ˮ�У�2Na+2H2O�T2Na++2OH-+H2�� | |
| D�� | ���ˮ�еμ�FeCl3��Һ�Ʊ�Fe��OH��3���壺Fe3++H2O�TFe��OH��3��+3H+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| t/min | 0 | 2 | 4 | 6 |
| n��Cl2��/10-3 mol | 0 | 1.8 | 3.7 | 5.4 |
| A�� | 0��2 min�ķ�Ӧ����С��4��6 min�ķ�Ӧ���� | |
| B�� | 2��6 min��Cl2��ʾ�ķ�Ӧ����Ϊ0.9 mol/��L•min�� | |
| C�� | ����ѹǿ�������HClת���� | |
| D�� | ƽ�ⳣ��K��200�棩��K��400�棩 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | x��y | B�� | x��y | C�� | x��y | D�� | ���ж� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
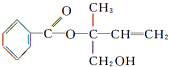
| A�� | X�ķ���ʽΪC12H16O3 | |
| B�� | �������Ը��������Һ���ֱ���X | |
| C�� | ������������ת���л���X��һ����ͬһƽ���ϵ�̼ԭ����Ϊ8 | |
| D�� | ��Ni�������������£�1 mol X���ֻ����1 mol H2�ӳ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ʵ�ˮ������ڷ�����ᴿ������ | |
| B�� | ��ϩ�������ͨ�����۷�Ӧ���ɸ߷��ӻ����� | |
| C�� | �л���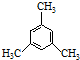 �ĺ˴Ź��������������壬�ҷ����֮��Ϊ3��1 �ĺ˴Ź��������������壬�ҷ����֮��Ϊ3��1 | |
| D�� | ���Ҵ���Ũ�����Ʊ���ϩʱ������ˮԡ���ȿ��Ʒ�Ӧ���¶� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
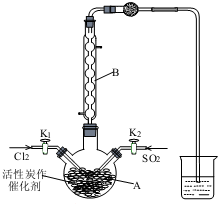 �����ȣ�SO2Cl2�������л��ϳɡ�ҽҩ��Ⱦ�ϡ�ũҩ�ȣ�Ҳ����������Լ����۵�-54.1�棬�е�69.1�棬��ˮ��������ˮ�⣮ijѧϰС������ͼװ���Ʊ������ȣ�����֪��SO2��g��+Cl2��g��?SO2Cl2��l����H��0����
�����ȣ�SO2Cl2�������л��ϳɡ�ҽҩ��Ⱦ�ϡ�ũҩ�ȣ�Ҳ����������Լ����۵�-54.1�棬�е�69.1�棬��ˮ��������ˮ�⣮ijѧϰС������ͼװ���Ʊ������ȣ�����֪��SO2��g��+Cl2��g��?SO2Cl2��l����H��0�����鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com