
【题目】铁、钛、镍等过渡元素在工业生产和科学研究中具有重要作用,请回答下列问题。
(1)有机铁肥[Fe(H2NCONH2)6](NO3)3的名称叫三硝酸六尿素合铁,是一种配合物,它的中心离子Fe3+的价电子排布式为____________;该配合物中N原子的杂化方式有_______________;它所含非金属元素的电负性由小到大的顺序是__________________。
(2)钛被称为继铁、铝之后的“第三金属”,也叫“未来金属”。
①钛位于周期表的_______区,基态Ti原子的电子占据了____________个原子轨道。
②工业上可用TiCl4(常温下呈液态)与Mg高温下反应制备钛单质,同时生成MgCl2,详细解释TiCl4熔点比MgCl2低很多的原因 _______________________________________________________ 。
(3)镍与CO生成的配合物Ni(CO)4中,易提供孤电子对的成键原子是_______________(填元素名称);1molNi(CO)4中含有的σ键数目为_________________ ;写出与CO互为等电子体的一种离子的化学式___________。
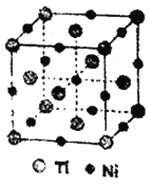
(4)镍钛记忆合金用于飞机和字宙飞船。已知一种钛镍合金的晶胞结构如图所示,其中Ti原子采用面心立方最密堆积方式,该合金中与Ti原子距离最近且相等的Ni原子个数为________;若合金的密度为ρg/cm3,NA代表阿伏加德罗常数的值,则晶胞中两个钛原子间的最近距离是____________pm。(用含ρ和NA的计算式表示,不必化简)
【答案】 3d5 sp3杂化和sp2杂化 H<C<N﹤O d 12 TiCl4属于分子晶体,熔融时破坏分子间作用力;而MgCl2属于离子晶体,熔融时破坏离子键,分子间作用力比离子键弱得多,所以TiCl4熔点低得多。 碳 8NA CN-或C22- 6 ![]() ×
×![]() ×1010
×1010
【解析】(1)Fe元素为26号元素,原子核外有26个电子,所以核外电子排布式为:1s22s22p63s23p63d64s2,铁原子失去最外层4s能级2个电子,然后失去3d能级上的1个电子形成Fe3+,Fe3+的电子排布式为1s22s22p63s23p63d5,所以基态Fe3+的价电子排布式为3d5;
由尿素分子的结构式H2NCONH2可知,尿素分子中N原子成3个单键,含有1对孤对电子,杂化轨道数为4,N原子采取sp3杂化;NO3-中含有3对价层电子对,其离子构型为平面三角形,N原子采取sp2杂化;元素非金属性越强电负性越大,故电负性H<C<N﹤O;(2)①钛位于周期表的d区,Ti原子核外电子数为22,基态原子核外电子排布为1s22s22p63s23p63d24s2,电子占据的原子轨道数为1+1+3+1+3+2+1=12个;②TiCl4属于分子晶体,熔融时破坏分子间作用力;而MgCl2属于离子晶体,熔融时破坏离子键,分子间作用力比离子键弱得多,所以TiCl4熔点低得多,工业上可用TiCl4(常温下呈液态)与Mg高温下反应制备钛单质,同时生成MgCl2;(3)配合物Ni(CO)4的中心原子Ni与CO之间的化学键称为配位键,提供孤电子对的成键原子是碳原子;Ni(CO)4中的配离子中Ni原子和C原子之间有4个σ键,CO分子中C和O之间存在1个σ键,1个π键,1个配位键,因此4个CO有4个σ键,故1mol Ni(CO)4中含有8molσ键即8NA;CO分子中含有2个原子、价电子数是10,与CO互为等电子体的与CO互为等电子体的阴离子微粒有CN-或C22-;(4)Ti原子采用面心立方最密堆积方式,若以Ti在面心,则合金中与Ti原子距离最近且相等的Ni原子在棱,个数为6;利用均摊法计算,每个晶胞中含有Ti8×![]() 个,Ni12×
个,Ni12×![]() 个,若合金的密度为ρg/cm3,NA代表阿伏加德罗常数的值,则晶胞体积为V=
个,若合金的密度为ρg/cm3,NA代表阿伏加德罗常数的值,则晶胞体积为V= cm3,边长为
cm3,边长为![]() cm,两个钛原子间的最近距离是边长的
cm,两个钛原子间的最近距离是边长的![]() ,为
,为![]() ×
×![]() cm=
cm=![]() ×
×![]() ×1010pm。
×1010pm。


 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是 ( )
A.2.7g金属铝变为铝离子时得到的电子数目为0.3NA
B.0.5molO3与11.2L O2所含的分子数一定相等
C.14g由乙烯(C2H4)和丙烯(C3H6)组成的混合物中含有原子的数目为3NA
D.22.4LCO2与CO的混合气体中含碳原子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知有五种元素的原子序数的大小顺序为C>A>B>D>E,A、C同周期,B、C同主族;A与B形成的离子化合物A2B中所有离子的电子数都相同,其电子总数为30;D和E可形成4核10电子分子。试回答下列问题:
(1)C两种元素的名称分别为________。
(2)用电子式表示离子化合物A2B的形成过程:_______________。
(3)写出D元素形成的单质的结构式:________________________。
(4)写出下列物质的电子式:
A、B、E形成的化合物:________________;D、E形成的化合物:__________________。
(5)A、B两种元素组成的化合物A2B2属于________(填“离子”或“共价”)化合物,存在的化学键类型是____________;写出A2B2与水反应的化学方程式:___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前海水液化可采用双极膜电液析法、同时获得副产品,其模拟工作原理如图所示。其中双极膜(BP)是阴、阳复合膜,在直流电的作用下,阴、阳膜复合层间的H2O解离成H+和OH-,作为H+和OH-离子源。M、N为离子交换膜。下列说法正确的是( )

A. X电极为电解池的阴极,该电极反应式为:2H+-2e-=H2↑
B. 电子流向:电源负极→X电极→Y电极→电源正极
C. 电路中每转移1mol电子,X、Y两极共得到标准状况下16.8L的气体
D. M为阳离子交换膜,A室获得副产品NaOH;若去掉B室双极膜,B室产物不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,容器内某反应中M、N的物质的量随反应时间变化的曲线如下图,下列表述中正确的是

A. t3时,正反应速率大于逆反应速率
B. t2时,正逆反应速率相等,反应达到平衡状态
C. 化学方程式为:2M= N
D. t1时,N的浓度是M浓度的2倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学反应中的能量变化是由化学反应中旧化学健断裂时吸收的能量与化学健形成时放出的能量不同引起的。如图为N2(g)和O2(g)反应生成NO(g)过程中的能量变化,下列说法中正确的是

A. 1molN2(g)和1molO2(g)反应放出的能量为180kJ
B. 1molN2(g)和1molO2(g)具有的总能量小于2molNO(g)具有的总能量
C. 在1L的容器中发生反应.10min内N2减少了1mol,因此10min内的平均反应速率为v(NO)=0.1mol/(L·min)
D. NO是一种酸性氧化物,能与NaOH溶液反应生成盐和水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向CuSO4溶液中加入H2O2溶液,很快有大量气体逸出,同时放热,一段时间后,蓝色溶液变为红色浑浊(Cu2O),继续加入H2O2溶液,红色浑浊又变为蓝色溶液,这个反应可以反复多次。下列关于上述过程的说法不正确的是
A. Cu2+是H2O2分解反应的催化剂 B. H2O2只表现了氧化性
C. H2O2的电子式为: ![]() D. 发生了反应Cu2O + H2O2+4H+=2Cu2++3H2O
D. 发生了反应Cu2O + H2O2+4H+=2Cu2++3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯是合成食品外包装材料聚乙烯的单体,可以由丁烷裂解制备。
主反应:C4H10(g,正丁烷) ![]() C2H4(g)+C2H6(g)△H1
C2H4(g)+C2H6(g)△H1
副反应:C4H10 (g,正丁烷) ![]() CH4(g)+C3H6(g) △H2
CH4(g)+C3H6(g) △H2
回答下列问题:
(1)化学上,将稳定单质的能量定为0,生成稳定化合物时的释放或吸收能量生成热,生成热可表示该物质相对能量。下表为25℃、101kPa下几种有机物的生成热:
物质 | 曱烷 | 乙烷 | 乙烯 | 丙烯 | 正丁烷 | 异丁烷 |
生成热/kJ·mol-1 | -75 | -85 | 52 | 20 | -125 | -132 |
①表格中的物质,最稳定的是_________________(填结构简式)。
②上述反应中,△H1=______kJ/mol。
③书写热化学方程式时,要标明“同分异构体名称”,其理由是________________________。
(2)一定温度下,在恒容密闭容器中投入一定量正丁烷发生反应生成乙烯。
①下列情况表明该反应达到平衡状态的是_______(填代号)。
A.气体密度保持不变 B.[c(C2H4)·c(C2H6)]/ c(C4H10)保持不变
C.反应热不变 D.正丁烷分解速率和乙烷消耗速率相等
②为了同时提高反应速率和转化率,下列措施可采用的是_____(填代号)。
A.加入高效催化剂B.升高温度C.充入乙烷D.减小压强
(3)向密闭容器中充入丁烷,在一定条件(浓度、催化剂及压强等)下发生反应,测得乙烯产率与温度关系如图所示。温度高于600℃时,随若温度升高,乙烯产率降低,可能的原因是__________(填代号)。

A.平衡常数降低 B.活化能降低C.催化剂活性降低 D.副产物增多
(4)在一定温度下向1L恒容密闭容器中充入2mol正丁烷,反应生成乙烯和乙烷,经过10min达到平衡状态,测得平衡时气体压强是原来的1.75倍。
①0~10min内乙烯的生成速率v(C2H4)为________mol·L-1·min-1。
②上述条件下,该反应的平衡常数K为____________。
(5)丁烷-空气燃料电池以熔融的K2CO3为电解质,以具有催化作用和导电性能的稀土金属材料为电极。该燃料电池的负极反应式为______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物X、Y、Z的分子式均为C7H8,结构简式如下:
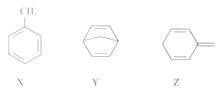
下列说法正确的是
A. X、Y、Z均为苯的同系物
B. X、Y、Z分子中的碳原子均处于同一平面
C. X、Y、Z均能使酸性高锰酸钾溶液褪色
D. 1molX、1molY分别与足量溴的四氯化碳溶液反应,均最多消耗2mol Br2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com