

 £»
£» £»
£» £»
£»
 £©
£© £ØĘäÖŠĮ½ÖÖ£©£ØČĪŠ“Į½ÖÖ£©
£ØĘäÖŠĮ½ÖÖ£©£ØČĪŠ“Į½ÖÖ£© ·ÖĪö AŗĶäå·¢ÉśČ”“ś·“Ӧɜ³ÉB£¬øł¾ŻBµÄ½į¹¹¼ņŹ½ÖŖ£¬AŹĒĮŚ¶ž¼×±½£¬ŌŚäå»ÆĢś×÷“߻ƼĮĢõ¼žĻĀ£¬ĮŚ¶ž¼×±½ŗĶäå·¢ÉśČ”“ś·“Ӧɜ³ÉC £¬B·¢ÉśŅ»ĻµĮŠ·“Ó¦ŗóÉś³ÉĮŚ±½¶ž¼×Č©£¬½įŗĻŅŃÖŖĢõ¼žÖŖ£¬ĮŚ±½¶ž¼×Č©·“Ӧɜ³ÉE£¬EµÄ½į¹¹¼ņŹ½ĪŖ
£¬B·¢ÉśŅ»ĻµĮŠ·“Ó¦ŗóÉś³ÉĮŚ±½¶ž¼×Č©£¬½įŗĻŅŃÖŖĢõ¼žÖŖ£¬ĮŚ±½¶ž¼×Č©·“Ӧɜ³ÉE£¬EµÄ½į¹¹¼ņŹ½ĪŖ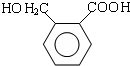 £¬E·¢ÉśĖõ¾Ū·“Ӧɜ³ÉF£¬FµÄ½į¹¹¼ņŹ½ĪŖ
£¬E·¢ÉśĖõ¾Ū·“Ӧɜ³ÉF£¬FµÄ½į¹¹¼ņŹ½ĪŖ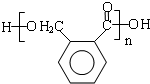 £¬½įŗĻĪļÖŹµÄŠŌÖŹĄ“·ÖĪö½ā“š£®
£¬½įŗĻĪļÖŹµÄŠŌÖŹĄ“·ÖĪö½ā“š£®
½ā“š ½ā£ŗAŗĶäå·¢ÉśČ”“ś·“Ӧɜ³ÉB£¬øł¾ŻBµÄ½į¹¹¼ņŹ½ÖŖ£¬AŹĒĮŚ¶ž¼×±½£¬ŌŚäå»ÆĢś×÷“߻ƼĮĢõ¼žĻĀ£¬ĮŚ¶ž¼×±½ŗĶäå·¢ÉśČ”“ś·“Ӧɜ³ÉC £¬B·¢ÉśŅ»ĻµĮŠ·“Ó¦ŗóÉś³ÉĮŚ±½¶ž¼×Č©£¬½įŗĻŅŃÖŖĢõ¼žÖŖ£¬ĮŚ±½¶ž¼×Č©·“Ӧɜ³ÉE£¬EµÄ½į¹¹¼ņŹ½ĪŖ
£¬B·¢ÉśŅ»ĻµĮŠ·“Ó¦ŗóÉś³ÉĮŚ±½¶ž¼×Č©£¬½įŗĻŅŃÖŖĢõ¼žÖŖ£¬ĮŚ±½¶ž¼×Č©·“Ӧɜ³ÉE£¬EµÄ½į¹¹¼ņŹ½ĪŖ £¬E·¢ÉśĖõ¾Ū·“Ӧɜ³ÉF£¬FµÄ½į¹¹¼ņŹ½ĪŖ
£¬E·¢ÉśĖõ¾Ū·“Ӧɜ³ÉF£¬FµÄ½į¹¹¼ņŹ½ĪŖ £¬
£¬
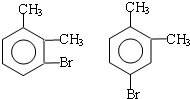
£Ø1£©AµÄ½į¹¹¼ņŹ½ĪŖ£ŗ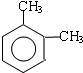 £¬ĘäĆū³ĘŹĒĮŚ¶ž¼×±½£¬¹Ź“š°øĪŖ£ŗĮŚ¶ž¼×±½£»
£¬ĘäĆū³ĘŹĒĮŚ¶ž¼×±½£¬¹Ź“š°øĪŖ£ŗĮŚ¶ž¼×±½£»
£Ø2£©ĮŚ¶ž¼×±½ŗĶäå·¢ÉśČ”“ś·“Ӧɜ³ÉB£¬ĮŚ¶ž¼×±½µÄ¼×»łÉĻĒāŌ×Ó±»äåŌ×ÓČ”“śÉś³Éäå“śĢž£¬ŌŚøĆ·“Ó¦µÄø±²śĪļÖŠ£¬ÓėB»„ĪŖĶ¬·ÖŅģ¹¹ĢåµÄ»ÆŗĻĪļµÄ½į¹¹¼ņŹ½ĪŖ £¬
£¬
¹Ź“š°øĪŖ£ŗČ”“ś·“Ó¦£» £»
£»
£Ø3£©ŌŚäå»ÆĢś×÷“߻ƼĮĢõ¼žĻĀ£¬ĮŚ¶ž¼×±½ŗĶäå·¢Éś±½»·ÉĻµÄČ”“ś·“Ó¦£¬Č”“śĪ»ÖĆĪŖ¼×»łµÄĮŚ”¢¶ŌĪ»£¬ĖłŅŌCæÉÄܵĽį¹¹¼ņŹ½ĪŖ£ŗ £¬
£¬
¹Ź“š°øĪŖ£ŗ £»
£»
£Ø4£©ĖįŠŌĢõ¼žĻĀ£¬ĮŚ¶ž¼×±½±»øßĆĢĖį¼ŲŃõ»ÆÉś³ÉĮŚ±½¶ž¼×Ėį£¬ŌŚÅØĮņĖį”¢¼ÓČČĢõ¼žĻĀ£¬ĮŚ±½¶ž¼×ĖįŗĶŅŅ“¼·¢Éśõ„»Æ·“Ӧɜ³ÉĮŚ±½¶ž¼×Ėį¶žŅŅõ„£¬ŗĻ³ÉĀ·ĻßĪŖ £¬
£¬
¹Ź“š°øĪŖ£ŗ £»
£»
£Ø5£©OPAµÄ»ÆѧĆū³ĘŹĒĮŚ±½¶ž¼×Č©£¬E·¢ÉśĖõ¾Ū·“Ӧɜ³ÉF£¬·¢Éś·“Ó¦µÄ¹ŁÄÜĶÅĪŖōĒ»łŗĶōČ»ł£¬øĆ·“Ó¦·½³ĢŹ½ĪŖ£ŗ £¬
£¬
¹Ź“š°øĪŖ£ŗōĒ»łŗĶōČ»ł£» £»
£»
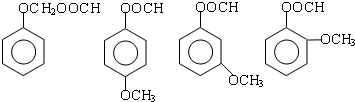
£Ø6£©EµÄ½į¹¹¼ņŹ½ĪŖ £¬·¼Ļć»ÆŗĻĪļGŹĒEµÄĶ¬·ÖŅģ¹¹Ģ壬G·Ö×ÓÖŠŗ¬ÓŠČ©»ł”¢õ„»łŗĶĆŃ»łČżÖÖŗ¬Ńõ¹ŁÄÜĶÅ£¬ŌņGµÄ½į¹¹¼ņŹ½æÉÄÜĪŖ£ŗ
£¬·¼Ļć»ÆŗĻĪļGŹĒEµÄĶ¬·ÖŅģ¹¹Ģ壬G·Ö×ÓÖŠŗ¬ÓŠČ©»ł”¢õ„»łŗĶĆŃ»łČżÖÖŗ¬Ńõ¹ŁÄÜĶÅ£¬ŌņGµÄ½į¹¹¼ņŹ½æÉÄÜĪŖ£ŗ £¬
£¬
¹Ź“š°øĪŖ£ŗ £ØĘäÖŠĮ½ÖÖ£©£®
£ØĘäÖŠĮ½ÖÖ£©£®
µćĘĄ ±¾Ģāæ¼²éÓŠ»śĪļµÄĶʶĻ£¬Ć÷Č·ÓŠ»śĪļµÄ¹ŁÄÜĶż°ĘäŠŌÖŹŹĒ½ā±¾Ģā¹Ų¼ü£¬ÄѶČÖŠµČ£¬ÄѵćŹĒĶ¬·ÖŅģ¹¹ĢåµÄŹéŠ“£¬×¢Ņā²»ÄܶąŠ“”¢Ā©Š“£®


 ĆūŠ£æĪĢĆĻµĮŠ“š°ø
ĆūŠ£æĪĢĆĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | BaCl2ČÜŅŗ | B£® | Ba£ØNO3£©2ČÜŅŗ | C£® | ÅØäåĖ® | D£® | ±„ŗĶNaHCO3ČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
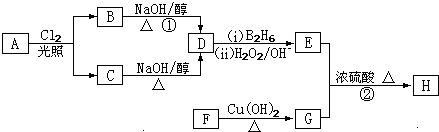
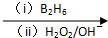 R-CH2CH2OH£ØB2 H6ĪŖŅŅÅšĶ飩
R-CH2CH2OH£ØB2 H6ĪŖŅŅÅšĶ飩 £»
£» £»
£»²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
| ŹµŃé²½Öč | Ō¤ĘŚĻÖĻóŗĶ½įĀŪ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1 mol SiO2¾§ĢåÖŠ£¬ŗ¬ÓŠ2NAøöSi-O¹²¼Ū¼ü | |
| B£® | ³£ĪĀĻĀ£¬4.4 g CO2ŗĶN2O»ģŗĻĪļÖŠĖłŗ¬ÓŠµÄŌ×ÓŹżĪŖ0.3 NA | |
| C£® | 0.2 mol Cl2Óė×ćĮæµÄĢś·Ū³ä·Ö·“Ó¦£¬×ŖŅʵē×ÓŹżĪŖ0.6NA | |
| D£® | ±ź×¼×“æöĻĀ£¬11.2 L ĀČ·ĀĖłŗ¬·Ö×ÓŹżĪŖ0.5 NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | KCl=K++Cl- | B£® | H2CO3?2 H++CO32- | ||
| C£® | H2SO4=2H++SO42- | D£® | Ba£ØOH£©2=Ba2++2OH- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
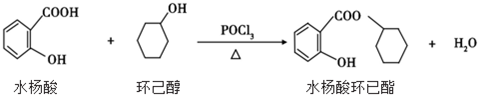
| A£® | Ė®ŃīĖįµÄŗĖ“Ź²ÕńĒāĘ×ÓŠ 4 øöĪüŹÕ·å | |
| B£® | Ė®ŃīĖį”¢»·ŅŃ“¼ŗĶĖ®ŃīĖį»·ŅŃõ„¶¼ÄÜÓė FeCl3 ČÜŅŗ·¢ÉśĻŌÉ«·“Ó¦ | |
| C£® | 1mol Ė®ŃīĖįøśÅØäåĖ®·“Ó¦Ź±£¬×ī¶ąĻūŗÄ 2molBr2 | |
| D£® | 1mol Ė®ŃīĖį»·ŅŃõ„ŌŚ NaOH ČÜŅŗÖŠĖ®½āŹ±£¬×ī¶ąĻūŗÄ 3molNaOH |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com