
分析 (1)根据燃烧产物为二氧化碳和水及质量守恒可知,该有机物分子中一定含有C、H元素;
(2)①根据n=$\frac{m}{M}$计算出该有机物及生成水的物质的量,然后根据质量守恒定律确定含有氧元素情况,最后确定分子式;
②根据分子式及“核磁共振氢谱检测该有机物共有三种氢”确定其结构简式;
③乙醇分子中含有羟基,能够与金属钠反应,能够发生酯化反应等.
解答 解:(1)燃烧4.6g某有机物,生成0.2molCO2和5.4g水,根据质量守恒可知,该有机物分子中一定含有C、H元素,不能确定是否含有氧元素,
故答案为:C、H;
(2)①4.6g该有机物的物质的量为:$\frac{4.6g}{46g/mol}$=0.1mol,该有机物分子中含有C原子数为:$\frac{0.2mol}{0.1mol}$=2;
5.4g水的物质的量为:$\frac{5.4g}{18g/mol}$=0.3mol,则该有机物分子中含有H原子数为:$\frac{0.3mol×2}{0.1mol}$=6,
含有C、H的总原子量为:12×2+1×6=30<46,则该有机物分子中一定含有氧元素,含有氧原子数目为:$\frac{46-30}{16}$=1,
则该有机物分子式为:C2H6O,
故答案为:C2H6O;
②分子式为C2H6O的有机物可能为乙醇或二甲醚,核磁共振氢谱检测该有机物共有三种氢,二甲醚只有1种H,则该有机物为乙醇:CH3CH2OH,
故答案为:CH3CH2OH;
③乙醇分子中含有羟基,能够与活泼金属钠反应:2CH3CH2OH+2Na→2CH3CH2ONa+H2↑;
乙醇和乙酸、浓硫酸共热发生酯化反应,反应方程式为:CH3COOH+CH3CH2OH$→_{△}^{浓硫酸}$CH3COOCH2CH3+H2O;
乙醇在银催化下与O2反应生成乙醛和水,反应方程式为:2CH3CH2OH+O2 $\stackrel{催化剂△}{→}$2CH3CHO+2H2O;
故答案为:乙醇能够与钠反应:2CH3CH2OH+2Na→2CH3CH2ONa+H2↑、乙醇发生酯化反应:CH3COOH+CH3CH2OH$→_{△}^{浓硫酸}$CH3COOCH2CH3+H2O、乙醇催化氧化生成乙醛2CH3CH2OH+O2 $\stackrel{催化剂△}{→}$2CH3CHO+2H2O等.
点评 本题考查了有机物结构与性质,题目难度中等,涉及有机物分子式确定的计算、有机物结构简式的判断、有机反应方程式书写等知识,熟练掌握常见有机物结构与性质为解答关键.


 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案科目:高中化学 来源: 题型:选择题
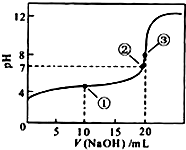 常温下,用0.1000mol•L-1NaOH溶液滴定 20.00mL0.1000mol•L-1CH3COOH溶液所得滴定曲线如图.下列说法正确的是( )
常温下,用0.1000mol•L-1NaOH溶液滴定 20.00mL0.1000mol•L-1CH3COOH溶液所得滴定曲线如图.下列说法正确的是( )| A. | 点①所示溶液中:c(CH3COO-)+c(OH-)=c(CH3COOH)+c(H+) | |
| B. | 点②所示溶液中:c(Na+)=c(CH3COOH)+c(CH3COO-) | |
| C. | 点③所示溶液中:c(Na+)>c(OH-)>c(CH3COO-)>c(H+) | |
| D. | 滴定过程中可能出现:c(CH3COOH)>c(CH3COO-)>c(Na+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
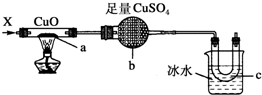
| A. | H2 | B. | CO和H2 | C. | NH3 | D. | CH3CH2OH(气) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 甲 | 乙 | 丙 | |
| 所含元素 | C、H | C、H、F | C、H、F |
| 所含电子数 | 26 | ||
| 结构特点 | 饱和有机物 | ||
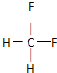 .下列关于乙的叙述正确的是D.
.下列关于乙的叙述正确的是D.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C、N、Si | B. | N、P、O | C. | N、O、S | D. | C、Si、S |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 反应 | 大气固氮 | 工业固氮 | |||
| N2(g)+02(g)? 2NO(g) | N2(g)+3H2 (g)?2NH3(g) | ||||
| 温度/℃ | 27 | 2000 | 25 | 400 | 450 |
| K | 3.84X10-31 | 0.1 | 5x103 | 0.507 | 0.152 |
| A. | 分析上表数据可知,大气固氮反应属于吸热反应 | |
| B. | 大气固氮正向反应K值太小,不适合大规模生产 | |
| C. | 从催化剂活性、反应速率等综合因索考虑,工业固氮应该选择适宜的温度 | |
| D. | 从平衡理论考虑,加压有利于氨的合成,所以在生产时压强越大越好 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com