
【题目】石油产品中除含有H2S外,还含有各种形态的有机硫,如COS、CH3SH。回答下列问题:
(1)CH3SH(甲硫醇)的电子式为________。
(2)一种脱硫工艺为:真空K2CO3—克劳斯法。
①K2CO3溶液吸收H2S的反应为K2CO3+H2S=KHS+KHCO3,该反应的平衡常数的对数值为lgK=_____(已知:H2CO3 lgK1=-6.4,lgK2=-10.3;H2SlgK1=-7,lgK2=-19)。
②已知下列热化学方程式:
a.2H2S(g)+3O2(g)=2SO2(g)+ 2H2O(l) △H1=-1172kJ/mol
b.2H2S(g)+O2(g)=2S(s)+2H2O(l) △H2=-632kJ/mol
克劳斯法回收硫的反应为SO2和H2S气体反应生成S(s),则该反应的热化学方程式为__________。
(3)Dalleska等人研究发现在强酸溶液中可用H2O2氧化COS。该脱除反应的化学方程式为______________。
(4)COS水解反应为COS(g)+H2O(g)![]() CO2(g)+H2S(g) △H=-35.5kJ/mol。
CO2(g)+H2S(g) △H=-35.5kJ/mol。
用活性α-Al2O3催化,在其它条件相同时,改变反应温度,测得COS水解转化率如图1所示;某温度时,在恒容密闭容器中投入0.3molH2O(g)和0.1molCOS,COS的平衡转化率如图2所示。
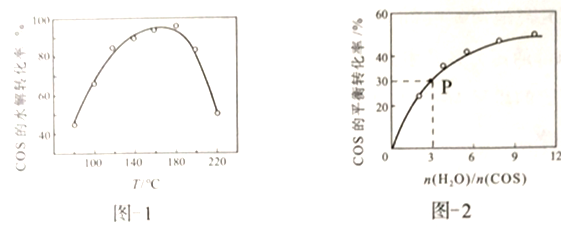
①图1活性α-Al2O3催化水解,随温度升高转化率先增大后又减小的可能原因是________。
②由图2可知,P点时平衡常数为K=______(填数字)。
③活性α-Al2O3催化水解,为提高COS的转化率可采取的措施是____________。
【答案】 ![]() 3.3 2H2S(g) + SO2(g) = 3S(s) +2H2O(l) △H=-362 kJ·mol-1 COS+4H2O2 =CO2+H2SO4+3H2O 开始温度低,催化剂活性小,到160℃活化剂活性最大,继续升温,催化剂活性降低且平衡向逆反应方向移动 0.0476 控制温度约160℃并增大n(H2O)/n(COS)
3.3 2H2S(g) + SO2(g) = 3S(s) +2H2O(l) △H=-362 kJ·mol-1 COS+4H2O2 =CO2+H2SO4+3H2O 开始温度低,催化剂活性小,到160℃活化剂活性最大,继续升温,催化剂活性降低且平衡向逆反应方向移动 0.0476 控制温度约160℃并增大n(H2O)/n(COS)
【解析】(1)CH3SH(甲硫醇)属于共价化合物,其电子式为![]() 。
。
(2)一种脱硫工艺为:真空K2CO3—克劳斯法。
① K2CO3+H2S=KHS+KHCO3
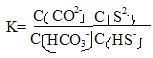 =
=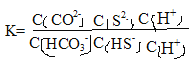 =
=![]() =10-7/10-10.3=103.3 lgK=3.3。答案:3.3。
=10-7/10-10.3=103.3 lgK=3.3。答案:3.3。
②已知下列热化学方程式:
根据a.2H2S(g)+3O2(g)=2SO2(g)+ 2H2O(l) △H1=-1172kJ/mol
b.2H2S(g)+O2(g)=2S(s)+2H2O(l) △H2=-632kJ/mol
![]() =-632 kJ/mol
=-632 kJ/mol![]() 3-(-1172kJ/mol)/2=-362 kJ·mol-1
3-(-1172kJ/mol)/2=-362 kJ·mol-1
故2H2S(g) + SO2(g) = 3S(s) +2H2O(l) △H=-362 kJ·mol-1
克劳斯法回收硫的反应为SO2和H2S气体反应生成S(s),则该反应的热化学方程式为2H2S(g) + SO2(g) = 3S(s) +2H2O(l) △H=-362 kJ·mol-1。
(3)Dalleska等人研究发现在强酸溶液中可用H2O2氧化COS。该脱除反应的化学方程式为COS+4H2O2 =CO2+H2SO4+3H2O
(4)①图1活性α-Al2O3催化水解,催化剂与温度有一个临界点,高于这个临界点,催化剂的活性降低。由图可知开始温度低,催化剂活性小,到160℃活化剂活性最大,继续升温,催化剂活性降低且平衡向逆反应方向移动。
② COS(g)+H2O(g)![]() CO2(g)+H2S(g
CO2(g)+H2S(g
初始量 0.1 0.3 0 0
变化量 X X X X
平衡量 0.1-X 0.3-X X X
P点时COS转化率为30![]() ,所以X=0.03mol平衡常数为K=0.3
,所以X=0.03mol平衡常数为K=0.3![]() 0.3/0.07
0.3/0.07![]() 0.27=0.0476
0.27=0.0476
③COS(g)+H2O(g)![]() CO2(g)+H2S(g) △H=-35.5kJ/mol。为提高可使化学平衡向正反应方向移动,根据影响化学平衡移动的因素温度,压强 浓度,由方程式可知压强不能改变平衡移动,所以可以增加水蒸气的浓度,温度升高COS的转化率降低,所以控制温度约160℃并增大n(H2O)/n(COS)即可。
CO2(g)+H2S(g) △H=-35.5kJ/mol。为提高可使化学平衡向正反应方向移动,根据影响化学平衡移动的因素温度,压强 浓度,由方程式可知压强不能改变平衡移动,所以可以增加水蒸气的浓度,温度升高COS的转化率降低,所以控制温度约160℃并增大n(H2O)/n(COS)即可。


科目:高中化学 来源: 题型:
【题目】甲图是生物体内四种有机物的组成与功能关系图,乙图是二糖的组成图,请据图回答下列问题。

(1)构成细胞的最基本元素是_____________,生物体内含量最多的有机化合物是图中的_______(填字母)
(2)甲图中物质D的基本元素组成是________;物质C的不同取决于_________的不同。
(3)小麦种子细胞中,物质E是指__________________。
(4)相同质量的E和F彻底氧化分解,耗氧量较多的是_____________。
(5)乙图B、C代表的单糖分别是_______、___________(填写具体名称)。不能水解的糖类是_____糖,构成淀粉、纤维素、糖原等多糖的单体都是____________________。
(6)淀粉→麦芽糖→葡萄糖→糖原,这是某生物体内糖类的某些变化,此生物一定是________(填“动物”或“植物”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.NH3的水溶液能导电,所以NH3是电解质
B.BaSO4其水溶液几乎不导电,但BaSO4是电解质
C.液溴不导电,所以液溴是非电解质
D.食盐水能导电,故其属于电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】最近报道的一种处理垃圾渗滤液并用其发电的示意图如下。装置工作时,下列说法不正确的是
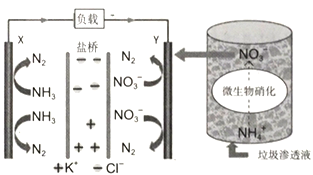
A. 盐桥中Cl-向Y极移动
B. 化学能转变为电能
C. 电子由X极沿导线流向Y极
D. Y极发生的反应为2NO3-+10e-+12H+=N2+6H2O,周围pH增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)
后使用。请回答下列问题:

(1)该“84消毒液”的物质的量浓度约为_____mol·L-1。
(2)取用任意体积的该盐溶液时,下列物理量中会随所取体积的多少而变化的是________(填字母)。
A.溶液中NaClO的物质的量 B.溶液的浓度
C.溶液中NaClO的摩尔质量 D.溶液的密度
(3)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480 mL含NaClO质量分数为25%的消毒液。回答下列问题。
①如图所示的仪器中,有些是不需要,配制上述溶液还需要_____________玻璃仪器

②需要称量NaClO固体的质量为_______ g
(4)“84消毒液”与稀硫酸混合使用可增强消毒能力,某消毒小组人员用98%(密度为1.84 g·cm-3)的浓硫酸配制200 mL 2.3 mol·L-1的稀硫酸用于增强“84消毒液”的消毒能力。
①所配制的稀硫酸中,H+的物质的量浓度为________ mol·L-1。
②需用浓硫酸的体积为________ mL。
③若所配制的稀硫酸浓度偏小,则下列可能的原因分析中正确的是_______。
A.配制前,容量瓶中有少量蒸馏水 B.量取浓硫酸时,仰视液体的凹液面
C.未冷却,立即转移至容量瓶定容 D.定容时,仰视溶液的凹液面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是:
A. Fe的摩尔质量为56g/mol
B. 通常状况下,18g水中含有1mol水分子
C. 0.1mol/L NaCl溶液中含Na+的物质的量为0.1mol
D. 标准状况下,11.2L O2与N2的混合气中含有的分子个数为3.01×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】自然界中的物质绝大多数以混合物的形式存在,为了便于研究和利用,常需对混合物进行分离和提纯。下列A、B、C、D是中学常见的混合物分离或提纯的装置。
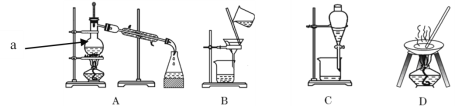
I.请根据混合物分离或提纯的原理,回答在下列实验中需要使用哪种装置。将A、B、C、D 填入适当的空格中。
(1)碳酸钙悬浊液中分离出碳酸钙___________;
(2)氯化钠溶液中分离出氯化钠___________;
(3)分离植物油和水___________;
(4)海水淡化___________;
(5)氯化钠溶液中分离出水___________;
(6)除去自来水中的Cl﹣等杂质___________;
(7)从碘水中分离出I2___________。
II.碘水中提取碘单质的方法如下:
(1)萃取分液
①下列可作为碘水中提取碘单质萃取剂的是___________
A.酒精 B.苯
②分液漏斗在使用前必须先___________
③查资料得知:ρ(H2O)>ρ(苯)>ρ(酒精),若用①中所选萃取剂萃取碘水中的碘单质,分液时,水层应由分液漏斗的______端口放出,有机层应由分液漏斗的______端口放出(此问填“上”或者“下”)
(2)蒸馏
①装置A中a的名称是_______,冷凝装置中冷凝水应该________口进(填“上”或“下”),
这样做的目的是________________________,装置C在分液时为使液体顺利滴下,除打开漏斗下端的旋塞外,还应进行的具体操作是__________________________。
②已知碘和四氯化碳的熔沸点数据如下表
熔点 | 沸点 | |
碘 | 113.7℃ | 184.3℃ |
四氯化碳 | -22.6℃ | 76.8℃ |
若用蒸馏法分离碘和四氯化碳的混合物,锥形瓶中先收集到的物质的名称是___________。
Ⅲ. 海水中蕴藏着丰富的资源,在实验室中取少量海水,进行如下流程的实验:
[海水]![]() [粗盐]
[粗盐]![]() [食盐水]→[氯化钠晶体]
[食盐水]→[氯化钠晶体]
问题一:粗盐中含Ca2+、Mg2+、SO42﹣等杂质,需要提纯后才能综合利用。粗盐提纯的步骤有:
①加入过量的Na2CO3溶液 ②加入过量的BaCl2溶液 ③加入过量的NaOH溶液 ④调节溶液的pH等于7 ⑤溶解 ⑥过滤 ⑦蒸发正确的操作顺序是__________(填选项字母).
a.⑤②③①⑥④⑦ b.⑤①②③⑥④⑦ c.⑤②①③④⑥⑦ d.⑤③②①⑥④⑦
问题二:由海水到氯化钠晶体的实验过程中要用到的主要装置是_________________(从给定的四种装置中选择,填字母)。
问题三:粗盐中含有少量泥沙、CaCl2、MgCl2及硫酸盐,将粗盐溶解后,先过滤将泥沙除去,再检验滤液中的SO42﹣,检验滤液中的SO42﹣的实验操作和现象是______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子一定能大量共存的是( )
A. 在强碱溶液中:Na+、K+、AlO2﹣、CO32﹣
B. 在pH=0的溶液中:K+、Fe2+、Cl﹣、NO3﹣
C. 在含大量Fe3+的溶液中:NH4+、Na+、Cl﹣、SCN﹣
D. 在c(H+)=10﹣13mol/L的溶液中:NH4+、Al3+、SO42﹣、NO3﹣
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com