
| A. | 加稀盐酸后过滤,除去混在铜粉中的少量镁粉和铝粉 | |
| B. | 加入氢氧化钠溶液,通过分液的方法,可以除去苯中的乙酸 | |
| C. | 将氢气和氧气的混合气体通过灼热的氧化铜,以除去其中的氢气 | |
| D. | 用萃取的方法分离汽油和煤油 |
分析 A.Mg、Al均与盐酸反应,而Cu不能;
B.乙酸与NaOH反应后,与苯分层;
C.氢气还原CuO后,Cu易被氧气氧化;
D.汽油和煤油互溶,但沸点不同.
解答 解:A.Mg、Al均与盐酸反应,而Cu不能,则加稀盐酸后过滤,除去混在铜粉中的少量镁粉和铝粉,故A正确;
B.乙酸与NaOH反应后,与苯分层,然后分液可分离,故B正确;
C.氢气还原CuO后,Cu易被氧气氧化,则通过灼热的氧化铜不能除杂,故C错误;
D.汽油和煤油互溶,但沸点不同,则应选择蒸馏法分离,故D错误;
故选AB.
点评 本题考查化学实验方案的评价,为高频考点,把握混合物分离原理、实验技能等等为解答的关键,侧重分析与实验能力的考查,题目难度不大.


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:解答题
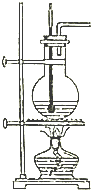 实验室用如图所示装置制取乙烯,请回答下列有关该实验的问题:
实验室用如图所示装置制取乙烯,请回答下列有关该实验的问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
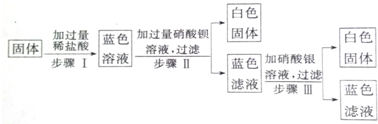
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
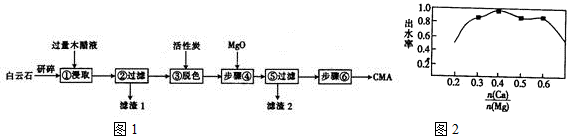
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 灼烧的铁丝在氯气中燃烧,集气瓶内充满棕黄色烟雾 | |
| B. | 氢气在氯气中燃烧,集气瓶口有白雾 | |
| C. | 向盛水的烧杯中先加入过氧化钠,再滴加酚酞,最终溶液呈红色 | |
| D. | 将一块钠放在燃烧匙中加热,燃烧后得到白色固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2发生还原反应 | B. | H2是还原剂 | C. | Cl2被氧化 | D. | Cl2发生氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 步骤 | 操 作 | 现 象 |
| ① | 用pH试纸检验 | 溶液的pH大于7 |
| ② | 向溶液中滴加氯水,再加入CCl4振荡,静置 | CCl4层呈橙色 |
| ③ | 向②所得溶液中加入Ba(NO3)2溶液和稀HNO3 | 有白色沉淀产生 |
| ④ | 将③过滤,向滤液中加入AgNO3溶液和稀HNO3 | 有白色沉淀产生 |
| A. | 可能含有的离子是①③⑥ | B. | 肯定没有的离子只有② | ||
| C. | 不能确定的离子只有⑤ | D. | 肯定含有的离子是①③④⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com