
【题目】化学与生活息息相关。下列说法正确的是( )
A.A12O3作耐火材料是因为氧化铝熔点高
B.医疗上,碳酸氢钠是治疗胃穿孔的一种药剂
C.铁在潮湿的空气中放置,易发生化学腐蚀而生锈
D.石英、水晶、水泥、光导纤维等物质的主要成分是SiO2
科目:高中化学 来源: 题型:
【题目】某无色透明溶液中,能大量共存的离子组是 :( )
A.Na、K+、SO42-、HCO3
B.Cu 2+、K+、SO42-、NO3-
C.NH4+、K+、Cl-、OH
D.Fe3+、K+、SCN-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:
(1)联氨分子的电子式为_____________,HCN中C的化合价为____________。
(2)实验室可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为___________。
(3)①2O2(g)+N2(g)=N2O4(l) ΔH1
②N2(g)+2H2(g)=N2H4(l) ΔH2
③O2(g)+2H2(g)=2H2O(g) ΔH3
④2N2H4(l) + N2O4(l)= 3N2(g)+ 4H2O(g) ΔH 4=-1048.9kJ/mol
上述反应热效应之间的关系式为ΔH4=_________,联氨和N2O4可作为火箭推进剂的主要原因为__________________。
(4)联氨为二元弱碱,在水中的电离方程式与氨相似,联氨在水中第一步电离反应的平衡常数值为______________(已知:N2H4+H+![]() N2H5+的K=8.7×107;KW=1.0×10-14)。联氨与硫酸形成的正盐的化学式为 。
N2H5+的K=8.7×107;KW=1.0×10-14)。联氨与硫酸形成的正盐的化学式为 。
(5)联氨是一种常用的还原剂。向装有少量AgBr的试管中加入联氨溶液,观察到的现象是 _。联氨可用于处理高压锅炉水中的氧气,防止锅炉被腐蚀。理论上1kg的联氨可除去水中溶解的O2___________kg;与使用Na2SO3处理水中溶解的O2相比,联氨的优点是 _。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向体积均为10 mL且物质的量浓度相同的两份NaOH溶液中分别通入一定量的CO2得到溶液甲和乙;向甲、乙两溶液中分别滴加0.1 mol·L-1盐酸,此时反应生成CO2体积(标准状况)与所加盐酸体积间的关系如图所示。则下列叙述中正确的是( )
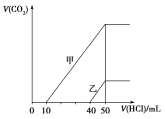
A.原NaOH溶液的物质的量浓度为0.5 mol·L-1
B.当0<V(HCl)<10 mL时,甲溶液中发生反应的离子方程式为:OH-+H+===H2O
C.乙溶液中含有的溶质是NaOH、NaHCO3
D.乙溶液中滴加盐酸后产生CO2体积的最大值为112 mL(标准状况)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F为原子序数依次增大的六种元素,A的一种同位素可用于考古测定生物的死亡年代,C原子的最外层电子数是次外层的3倍,D与B同主族;E的原子序数是A、B之和的2倍;F的原子序数为29。回答下列问题:
(1)六种元素中第一电离能最大的是 (填元素符号),其中D原子价电子排布图为 。
(2)基态E原子核外未成对电子数为 。
(3)BC2-的立体构型为 ,与其互为等电子体的分子是 (写化学式)。
(4)FC在加热条件下容易转化为F2C,从原子结构的角度解释原因 ;F晶体的堆积方式为 (填序号)。
①简单立方堆积 ②体心立方堆枳 ③六方最密堆积 ④面心立方最密堆积
(5)硼与D可形成一种耐磨材料G,其结构与金刚石相似(如图),可由硼的三溴化物和D的三溴化物高温下在氢气的氛围中合成。G的晶胞边长为a Pm,则该晶体密度的表达式为 g· cm﹣3(含a、NA的式子表示,不必化简)。
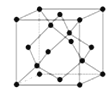
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I. 钛被称为继铁、铝之后的第三金属,制备金属钛的一种流程如下:
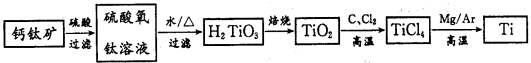
回答下列问题:
(1)已知TiCl4在通常情况下是无色液体,熔点为-37℃,沸点为136℃,可知TiCl4为___________晶体。
(2)钙钛矿晶体的结构如图所示。钛离子位于立方晶胞的角顶,被____个氧离子包围成配位八面体;钙离子位于立方晶胞的体心,被____个氧离子包围。
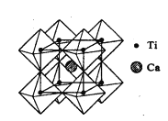
(3)纳米TiO2是一种应用广泛的催化剂,其催化的一个实例如下:
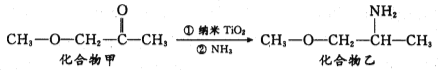
化合物甲中C原子的杂化方式为_______________;化合物乙的沸点明显高于化合物甲,主要原因是_______________________________。
II. 金属镍及其化合物在合金材料以及催化剂等方面应用广泛。请回答下列问题:
(4)镍元素在元素周期表中的位置为 。
(5)NiO、FeO的晶体结构类型均与氯化钠的相同,Ni2+和Fe2+的离子半径分别为69 pm和78 pm,则熔点NiO________FeO(填“<”或“>”);
(6)甲醛(H2C=O)在Ni催化作用下加氢可得甲醇(CH3OH)。甲醇分子内的O—C—H键角______(填“大于”“等于”或“小于”)甲醛分子内的O—C—H键角。
(7)Ni的氯化物与氨水反应可形成配合物[Ni(NH3)4]Cl2,2mol该配合物中含有σ键______mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的转化在给定条件下能实现的是( )
A.NaCl(aq)![]() NaHCO3(s)
NaHCO3(s) ![]() Na2CO3(s)
Na2CO3(s)
B.CuCl2![]() Cu(OH)2
Cu(OH)2![]() Cu
Cu
C.Al ![]() NaAlO2(aq)
NaAlO2(aq) ![]() NaAlO2(s)
NaAlO2(s)
D.MgO(s)![]() Mg(NO3)2(aq)
Mg(NO3)2(aq) ![]() Mg(s)
Mg(s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列各组物质:
A.金刚石与石墨;
B.淀粉与纤维素;
C.氕与氘;
D.甲烷与戊烷;
E.葡萄糖与果糖
F.![]() 与
与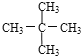
G.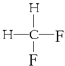 与
与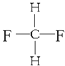
其中互为同位素 ;(填编号.下同),互为同系物的是 ,互为同分异构体的是 ,是同一种物质的是 .
(2)120℃,101kpa下,9ml由CO和C2H4组成的混合气体在足量的O2中完全燃烧后,恢复到原温度和压强.测得混合气体完全燃烧所消耗O2的体积与生成CO2的体积相等.请回答下列问题。
①等体积的CO和C2H4在相同条件下完全燃烧,生成CO2的体积比为 ;消耗O2的体积比为 .
②燃烧前混合气体中CO的体积为 , C2H4的体积为 .
(3)①化合物A的结构简式为: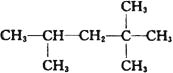 ,它是汽油燃烧品质抗震性能的参照物,其中A的同分异构体中含等效氢原子种类最少的一种结构简式为:_______________;若A是由烯烃和H2通过加成反应得到,则该烯烃的所有可能的结构简式为__________________。
,它是汽油燃烧品质抗震性能的参照物,其中A的同分异构体中含等效氢原子种类最少的一种结构简式为:_______________;若A是由烯烃和H2通过加成反应得到,则该烯烃的所有可能的结构简式为__________________。
②篮烷分子的键线式如图所示,试回答:
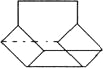
I写出篮烷分子的化学式____________;II篮烷分子的一氯取代物的种数为_______种。
(4)元素氮的一种液态氢化物叫肼,其分子中氮原子与氢原子个数比为1:2.肼﹣空气燃料电池是一种环保碱性燃料电池,其电解质溶液是20%﹣30%的KOH溶液.氮元素对应的燃烧产物为N2。该燃料电池的负极的电极反应式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A.氯气通入氯化亚铁溶液中:Cl2+Fe2+=2Cl-+Fe3+
B.钠投入水中:Na+H2O=H2↑+Na++OH-
C.漂白粉的漂白原理:2ClO-+CO2+H2O=CO32-+2HClO
D.用小苏打治疗胃酸过多:HCO3-+H+=H2O+CO2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com