
钛被称为“21世纪金属”,是研制卫星、火箭、宇宙飞船及深海潜艇的重要材料。研究发现,可以用石墨作阳极、钛网作阴极、熔融CaF2-CaO作电解质,利用如图所示装置模拟获得金属钙(需定期更换石墨棒),并以钙为还原剂,还原二氧化钛制备金属钛。下列叙述正确的是( )
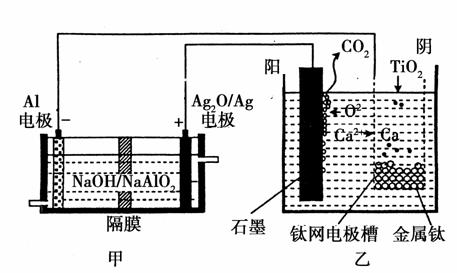
A.甲装置工作过程中OH-向Ag2O/Ag极移动,乙装置工作过程中O2-向阴极移动
B.若电解金属Ti效率为η,则制备1 mol Ti时消耗Al的物质的量为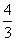 (1-η) mol
(1-η) mol
C.乙装置阳极的电极反应式为C+2O2--4e-===CO2↑
D.在制备金属钛前后,整套装置中CaO的总量减少
 特高级教师点拨系列答案
特高级教师点拨系列答案科目:高中化学 来源: 题型:
有关如图所示化合物的说法不正确的是( )
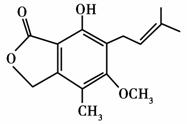
A.该有机物的分子式为C15H18O4
B.1 mol该化合物最多可以与2 mol NaOH反应
C.既可以催化加氢,又可以使酸性KMnO4溶液褪色
D.既可以与FeCl3溶液发生显色反应,又可以与NaHCO3溶液反应放出CO2气体
查看答案和解析>>
科目:高中化学 来源: 题型:
一种新型燃料电池,是用两根金属铂作电极插入KOH溶液中,然后向两极上分别通入CH3OH和O2,下列说法不正确的是( )
A.通入CH3OH的电极为负极
B.随着放电的进行,负极附近pH上升
C.每消耗1 mol CH3OH可以向外电路提供6 mol e-
D.通入O2的一极电极反应为2H2O+O2+4e-===4OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
500 mL NaNO3和Cu(NO3)2的混合溶液中c(NO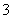 )=0.3 mol·L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到气体1.12 L(标准状况下),假定电解后溶液体积仍为500 mL,下列说法正确的是( )
)=0.3 mol·L-1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到气体1.12 L(标准状况下),假定电解后溶液体积仍为500 mL,下列说法正确的是( )
A.原混合溶液中c(Na+)=0.2 mol·L-1
B.电解后溶液中c(H+)=0.2 mol·L-1
C.上述电解过程中共转移0.4 mol电子
D.电解后得到的Cu的物质的量为0.1 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
甲烷是天然气的主要成分,是生产生活中应用非常广泛的一种化学物质。
(1)一定条件下,用甲烷可以消除氮氧化物(NOx)的污染。已知:
CH4(g)+4NO(g)===2N2(g)+CO2(g)+2H2O(g) ΔH1
CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(g) ΔH2
现有一份在相同条件下对H2的相对密度为17的NO与NO2的混合气体,用16 g甲烷气体催化还原该混合气体,恰好生成氮气、二氧化碳气体和水蒸气,共放出1042.8 kJ热量。
①该混合气体中NO和NO2的物质的量之比为________。
②已知上述热化学方程式中ΔH1=-1160 kJ/mol,则ΔH2=________。
③在一定条件下NO气体可以分解为NO2气体和N2气体,写出该反应的热化学方程式:______________。
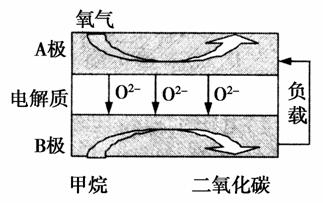
(2)以甲烷为燃料的新型电池,其成本大大低于以氢气为燃料的传统燃料电池,目前得到广泛地研究,如图是目前研究较多的一类固体氧化物燃料电池工作原理示意图。回答下列问题:
④B极为电池________极,电极反应式为________________。
⑤若用该燃料电池作电源,用石墨作电极电解100 mL 1 mol/L的硫酸铜溶液,写出阳极的电极反应式:_______________,当两极收集到的气体体积相等时,理论上消耗的甲烷的体积为______(标准状况下),实际上消耗的甲烷体积(折算到标准状况)比理论上大,可能原因为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在恒容的密闭容器中,可逆反应X(s)+3Y(g)2Z(g) ΔH>0,达到平衡时,下列说法正确的是( )
A.充入少量He使容器内压强增大,平衡向正反应方向移动
B.升高温度,平衡向正反应方向移动,容器内压强减小
C.继续加入少量X,X的转化率减小,Y的转化率增大
D.继续加入少量Y,再次平衡时,Y的体积分数比上次平衡小
查看答案和解析>>
科目:高中化学 来源: 题型:
下图中A~J分别代表相关反应的一种物质。已知A分解得到等物质的量的B、C、D,图中有部分生成物未标出。

请填写以下空白:
(1)A的化学式________。
(2)写出反应①②的化学方程式:
①_________________________________________ _______________________________,
_______________________________,
②________________________________________________________________________。
(3)写出反应③的离子方程式:____________________________________________。
(4)J与F反应的化学方程式:_______________________________________________。
(5)在反应④中,当生成标况下2.24 L G时,转移电子数为__________mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com