
下列关于原电池的叙述正确的是
A. 构成原电池的正极和负极必须是两种不同的金属
B. 原电池是将化学能转变为电能的装置
C. 在原电池中,电子流出的一极是负极,该电极被还原
D. 原电池放电时,电流的方向是从负极到正极
 互动英语系列答案
互动英语系列答案 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案科目:高中化学 来源: 题型:
下列各组离子一定能大量共存的是( )
A.在含有大量(AlO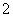 )的溶液中:NH
)的溶液中:NH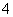 、Na+、Cl+、H+
、Na+、Cl+、H+
B.在强碱溶液中:Na+、K+、CO 、NO
、NO
C.在pH=12的溶液 中:NH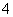 、Na+、SO
、Na+、SO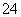 、Cl-
、Cl-
D.在c(H+)=0.1 mol·L-1的溶液中:K+、I-、Cl-、NO
查看答案和解析>>
科目:高中化学 来源: 题型:
已知一种c(H+)=1×10-3 mol·L-1的酸溶液和一种c(OH-)=1×10-3 mol·L-1的碱溶液等体积混合后,溶液呈酸性,其原因可能是( )
A.浓的强酸和稀的强碱溶液反应
B.浓的弱酸和稀的强碱溶液反应
C.等浓度的强酸和弱碱溶液反应
D.生成了一种强酸弱碱盐
查看答案和解析>>
科目:高中化学 来源: 题型:
今有下列四种酸溶液:(A)c(H+)=0.1 mol·L-1的盐酸,(B)c(H+)=0.1 mol·L-1的硫酸,(C)c(H+)=0.1 mol·L-1的醋酸,(D)0.01 mol·L-1的醋酸。
(1)四种酸中,c(H+)的大小关系是(用标号表示,下同)______________。
(2)四种溶液的溶质的物质的量浓度的大小关系是______。
(3)取等体积的四种溶液分别无限稀释,酸分子可电离生成的全部H+的物质的量的大小关系是__________________。
(4)取等体积的四种溶液,分别加入等量锌粉,刚开始反应时反应速率的大小关系是________________________________________________________________________;
当反应结束后,发现有一种酸有剩余,则此酸为__________。
(5)取等体积的四种溶液分别加入NaOH溶液,当完全中和时,消耗NaOH的物质的量的关系是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、M、N代表五种金属,有以下化学反应:
(1)水溶液中X+Y2+===X2++Y;
(2)Z+2H2O(冷水)===Z(OH)2+H2↑;
(3)M、N为电极,与N盐溶液组成原电池,M电极反应为M-2e-===M2+;
(4)Y可以溶于稀硫酸中,M不被稀硫酸氧化。
则这五种金属的活动性由弱到强的顺序是
A.M<N<Y<X<Z B.N<M<X<Y<Z C.N<M<Y<X<Z D.X<Z<N<M<Y
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,1 mol化学键断裂成气态原子所需消耗的能量用E表示。结合表中信息判断下列说法不正确的是
| 共价键 | H—H | F—F | H—F | H—Cl | H—I |
| E(kJ·mol-1) | 436 | 157 | 568 | 432 | 298 |
A.432 kJ·mol-1>E(H—Br)>298 kJ·mol-1
B.表中最稳定的共价键是H—F键
C.H2(g)―→2H(g) ΔH=+436 kJ·mol-1
D.H2(g)+F2(g)===2HF(g) ΔH=-25 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
某微粒的结构示意图为 ,下列有关该微粒的说法错误的是
,下列有关该微粒的说法错误的是
A.该微粒的原子核内有11个质子 B.该微粒在化学反应中最容易失去1个电子
C.该微粒的原子核外有3个电子层 D.该图表示的微粒是一种离子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com