
 某化学实验小组想要了解市场上所售食用白醋(主要是醋酸的水溶液)的酸度(酸度单位:g/100ml),现从市场上买来一瓶某品牌食用白醋,用实验室标准NaOH溶液对其进行滴定.下表是4种常见指示剂的变色范围:
某化学实验小组想要了解市场上所售食用白醋(主要是醋酸的水溶液)的酸度(酸度单位:g/100ml),现从市场上买来一瓶某品牌食用白醋,用实验室标准NaOH溶液对其进行滴定.下表是4种常见指示剂的变色范围:| 指示剂 | 石蕊 | 甲基橙 | 甲基红 | 酚酞 |
| 变色范围 (PH) | 5.0-8.0 | 3.1-4.4 | 4.4-6.2 | 8.2-10.0 |
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗NaOH溶液体积/ml | 26.02 | 25.32 | 25.28 |
分析 (1)根据醋酸和NaOH反应生成了强碱弱酸盐,溶液呈碱性,溶液呈碱性,应选择碱性变色范围内的指示剂;量取酸应该用酸式滴定管;
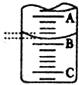
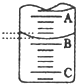
(2)A与C刻度间相差1ml,说明每两个小格之间是0.1mL,A处的刻度 25,据此确定B的刻度,注意滴定管的上面数值小,下面数值大;
(3)根据c(待测)=$\frac{c(标注)×V(标准)}{V(待测)}$分析不当操作对V(标准)的影响,以此判断浓度的误差;
(4)第一次消耗氢氧化钠溶液体积过大,应舍去,利用第二、三次消耗NaOH溶液的平均体积,利用平均值计算醋酸的质量,再根据酸度公式计算其酸度.
解答 解:(1)醋酸和NaOH反应生成了强碱弱酸盐,溶液呈碱性,应选择碱性变色范围内的指示剂,故选酚酞;白醋是酸性溶液,应该用酸式滴定管量取;
故答案为:酚酞;酸式滴定管;
(2)A与C刻度间相差1ml,说明每两个小格之间是0.10mL,A处的刻度为25,A和B之间是四个小格,所以相差0.40mL,则B是25.40mL,由于滴定管50.00mL刻度下方还有液体,所以实际溶液的液体大于24.60mL,
故答案为:25.40;大于24.60mL;
(3)从上表可以看出,第一次实验中记录消耗NaOH溶液体积明显多于后两次,上面测得的醋酸浓度偏大,
A.实验结束时俯视刻度线读取滴定终点时NaOH溶液的体积,造成V(标准)偏小,根据c(待测)=$\frac{c(标注)×V(标准)}{V(待测)}$分析,可知c(待测)偏小,故A错误;
B.滴定前滴定管尖嘴有气泡,滴定结束无气泡,造成V(标准)偏大,根据c(待测)=$\frac{c(标注)×V(标准)}{V(待测)}$分析,可知c(待测)偏大,故B正确;
C.盛装标准液的滴定管装液前用蒸馏水润洗过,未用标准液润洗,标准液被稀释,造成V(标准)偏大,根据c(待测)=$\frac{c(标注)×V(标准)}{V(待测)}$分析,可知c(待测)偏大,故C正确;
D.第一次滴定用的锥形瓶用待装液润洗过,后两次未润洗,润洗后待测液的物质的量偏多,造成V(标准)偏大,根据c(待测)=$\frac{c(标注)×V(标准)}{V(待测)}$分析,可知c(待测)偏大,故D正确;
E.滴定NaOH溶液过快,未充分振荡,刚看到溶液变色,立刻停止滴定,造成V(标准)偏小,根据c(待测)=$\frac{c(标注)×V(标准)}{V(待测)}$分析,可知c(待测)偏小,故E错误;
故选BCD;
(4)第一次数据相差较大,舍去,两次使用氢氧化钠溶液的平均体积=$\frac{25.32+25.28}{2}$mL,则醋酸的质量=$\frac{25.32+25.28}{2}$mL×10-3$\frac{L}{mL}$×Cmol/L×60g/mol,白醋体积为VmL,所以其酸度=$\frac{\frac{25.32+25.28}{2}×1{0}^{-3}×C×60}{V}$×100=$\frac{(25.28+25.32)×c×0.1×60}{2V}$;
故答案为:$\frac{(25.28+25.32)×c×0.1×60}{2V}$.
点评 本题考查酸碱滴定实验,误差分析,难度较大,会根据实际需要选取指示剂,关于酸度的计算为易错点.


 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案科目:高中化学 来源: 题型:解答题
| 烧杯和溶液的质量/g | 烧杯和剩余溶液的质量/g | 量筒中溶液的质量/g | 量筒中溶液的体积/cm3 | 硫酸铜溶液的密度ρ/(g•cm-3) |
| 49.2 | 28.2 | 21 | 20 | 1.05 |
查看答案和解析>>
科目:高中化学 来源:2017届福建省高三上第二次月考化学试卷(解析版) 题型:选择题
某化学小组为测定下列各混合物中铝的质量分数,设计了如下实验方案:
①铜铝混合物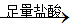 充分反应测定生成气体的体积
充分反应测定生成气体的体积
②铜铝混合物 充分反应测定剩余固体的质量
充分反应测定剩余固体的质量
③铜铝混合物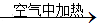 充分反应测定所得固体的质量
充分反应测定所得固体的质量
④铁铝混合物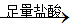 充分反应测定生成气体的体积
充分反应测定生成气体的体积
以上方案可行的是( )
A.①②③ B.②③④ C.①③④ D.①②③④
查看答案和解析>>
科目:高中化学 来源:2017届福建省高三上第二次月考化学试卷(解析版) 题型:选择题
下列各组中的两种物质作用时,反应条件(温度?反应物用量比)改变,不会引起产物的种类改变的是( )
A.Na和O2 B.NaOH和CO2
C.Na2O2和CO2 D.NaHCO3和Ca(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某化学实验小组想要了解市场上所售食用白醋(主要是醋酸的水溶液)的酸度,现从市场上买来一瓶某品牌食用白醋,用实验室标准NaOH溶液对其进行滴定.下表是4种常见指示剂的变色范围:
某化学实验小组想要了解市场上所售食用白醋(主要是醋酸的水溶液)的酸度,现从市场上买来一瓶某品牌食用白醋,用实验室标准NaOH溶液对其进行滴定.下表是4种常见指示剂的变色范围:| 指示剂 | 石蕊 | 甲基橙 | 甲基红 | 酚酞 |
| 变色范围(pH) | 5.0~8.0 | 3.1~4.4 | 4.4~6.2 | 8.2~10.0 |
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗NaOH溶液体积/mL | 26.02 | 25.32 | 25.28 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
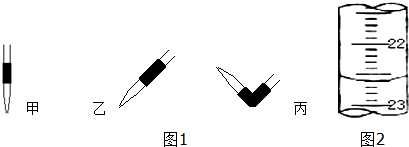
| 滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 20.00 | 0.50 | 25.40 |
| 第二次 | 20.00 | 4.00 | 29.10 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
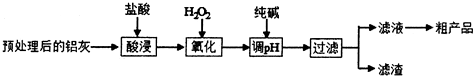
| 金属离子 | 开始沉淀的pH | 完全沉淀的pH |
| Fe3+ | 1.1 | 2.8 |
| A13+ | 3.4 | 4.7 |
| Fe2+ | 5.8 | 8.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 离子 | Cu2- | Al3+ | H+ | Cl- | SO42- |
| c(mol/L) | 1 | 1 | 2 | 3 | a |
| A. | 电路中共转移0.9mol电子 | B. | 铝元素以Al(OH)3的形式存在 | ||
| C. | 阴极质量增加3.2g | D. | a=2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com