
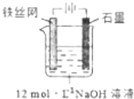
 高铁酸钾(K2FeO4)是一种高效多功能水处理剂,具有极强的氧化性.
高铁酸钾(K2FeO4)是一种高效多功能水处理剂,具有极强的氧化性.| 干法 | Fe2O3、KNO3、KOH混合加热共熔生成紫红色高铁酸盐和KNO2等产物 |
| 湿法 | 强碱性介质中,Fe(NO3)3与NaClO反应生成紫红色高铁酸盐溶液 |
| 电解法 | 制备中间产物Na2FeO4,再与KOH溶液反应 |
分析 (1)高铁酸钾(K2FeO4)具有极强的氧化性,是一种优良的水处理剂,起到杀菌消毒作用,形成胶体具有吸附悬浮杂质的作用;依高铁酸根离子水解平衡移动的影响因素解答;
(2)①Fe2O3、KNO3、KOH混合加热发生氧化还原反应,Fe元素化合价升高,化合价由+3价升高到+6价,被氧化,N元素化合价由+5价降低到+3价,依据氧化还原反应得失电子守恒规律计算;
②由信息可知,碱性介质中K2FeO4与Fe3+发生氧化还原反应生成K3FeO4,根据元素守恒还应生成H2O,反应中FeO42-→FeO43-,铁元素化合价由+6价降低为+5价,总共降低1价,Fe3+→FeO43-,铁元素化合价由+3价升高为+5价,总共升高2价,化合价升降最小公倍数为2,所以FeO42-系数为2,Fe3+系数为1,根据铁元素守恒确定FeO43-系数,根据电荷守恒确定OH-系数,根据氢元素守恒确定H2O系数,检查氧元素守恒,据此写出氧化还原反应方程式;
③电解时阳极Fe失电子发生氧化反应,被氧化生成高铁酸根离子;
(3)放电时,为原电池,依据3Zn+2K2FeO4+8H2O=3Zn(OH)2+2Fe(OH)3+4KOH,锌化合价升高,发生氧化反应,做负极,高铁酸根离子在正极得到电子,发生还原反应生成氢氧化铁;
(4)依据溶度积规则,当Qc=Ksp达到沉淀溶解平衡,要产生沉淀则Qc>Ksp,据此解答.
解答 解:(1)K2FeO4具有强氧化性,能够消毒杀菌;同时FeO42- 被还原成Fe3+,Fe3+水解形成Fe(OH)3胶体,能够吸附水中悬浮杂质;4FeO42-+10H2O?4Fe(OH)3+8OH-+3O2↑,增大溶液中的氢氧根离子浓度,能够使平衡逆向移动,抑制高铁酸根离子的水解,所以同浓度的高铁酸钾在pH为11.50的水溶液中最稳定;
故答案为:K2FeO4具有强氧化性,能够消毒杀菌;同时FeO42- 被还原成Fe3+,Fe3+水解形成Fe(OH)3胶体,能够吸附水中悬浮杂;11.50;
(2)①Fe元素化合价升高,化合价由+3价升高到+6价,被氧化,Fe2O3做还原剂;N元素化合价由+5价降低到+3价,KNO3做氧化剂,设氧化剂物质的量为xmol,还原剂物质的量为ymol,要使氧化剂得到电子总数等于还原剂失去电子总数,x×(5-3)=y×2×(6-3),解得x:y=3:1;
故答案为:3:1;
②由信息可知,碱性介质中K2FeO4与Fe3+发生氧化还原反应生成K3FeO4,根据元素守恒还应生成H2O,反应中FeO42-→FeO43-,铁元素化合价由+6价降低为+5价,总共降低1价,Fe3+→FeO43-,铁元素化合价由+3价升高为+5价,总共升高2价,化合价升降最小公倍数为2,所以FeO42-系数为2,Fe3+系数为1,根据铁元素守恒确定FeO43-系数为3,根据电荷守恒确定OH-系数8,根据氢元素守恒确定H2O系数为4,反应离子方程式为2FeO42-+Fe3++8OH-=3FeO43-+4H2O;
故答案为:2FeO42-+Fe3++8OH-=3FeO43-+4H2O;
③电解时阳极Fe失电子发生氧化反应,电极反应方程式为Fe+8OH--6e-═FeO42-+4H2O;
故答案为:Fe+8OH--6e-═FeO42-+4H2O;
(3)放电时,为原电池,依据3Zn+2K2FeO4+8H2O=3Zn(OH)2+2Fe(OH)3+4KOH,锌化合价升高,发生氧化反应,做负极,高铁酸根离子在正极得到电子,发生还原反应生成氢氧化铁,电极反应式为:FeO42-+4H2O+3e-═Fe(OH)3+5OH-;
故答案为:Zn;FeO42-+4H2O+3e-═Fe(OH)3+5OH-;
(4)设加入Ca(OH)2的物质的量为xmol,则溶液中钙离子浓度为x×10-3mol/L,含有2.0×l0-4 mol•L-lK2FeO4的废水中的c(FeO42-)=2.0×l0-4 mol•L-l,
Qc=x×10-3mol/L×2.0×l0-4 mol•L-l=Ksp=4.54×l0-9;
解得:x=2.27×10-2;
故答案为:2.27×10-2.
点评 本题为综合题,考查了氧化还原反应方程式的书写及配平、电极反应式的书写、溶度积规则的应用,题目难度较大,明确物质的性质及题给信息、熟悉化合物中各元素化合价、沉淀溶解平衡规律是解本题关键,氧化还原方程式的书写是难点.


科目:高中化学 来源: 题型:选择题
| A. | Na+、Cl-、Al3+、Ag+ | B. | $NH_4^+$、Mg2+、$NO_3^-$、$SO_4^{2-}$ | ||
| C. | K+、Ca2+、$NO_3^-$、$CO_3^{2-}$ | D. | $HCO_3^-$、Na+、K+、$SO_4^{2-}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
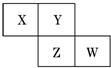 X、Y、Z、W均为短周期元素,它们在元素周期表中的相对位置如图所示.若Z原子的最外层电子数是第一层电子数的3倍,下列说法中正确的是( )
X、Y、Z、W均为短周期元素,它们在元素周期表中的相对位置如图所示.若Z原子的最外层电子数是第一层电子数的3倍,下列说法中正确的是( )| A. | X的最常见气态氢化物的水溶液显酸性 | |
| B. | 最高价氧化物对应水化物的酸性W比Z强 | |
| C. | Z的单质与氢气反应比Y单质与氢气反应剧烈 | |
| D. | X的原子半径小于Y |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将Fe(N03)2样品溶于稀H2SO4后,滴加KSCN溶液,溶液变红,则Fe(N03)2晶体已氧化变质 | |
| B. | 常温下,pH都为11的氢氧化钠溶液和氨水均加水稀释100倍,pH都变为9 | |
| C. | 25℃时,Ksp( BaC03)>Ksp( BaCrO4),则沉淀水体中的Ba2+选择Na2CrO4比Na2CO3好 | |
| D. | 将CH3CH2Br与NaOH溶液共热,冷却后取出上层溶液,加入AgNO3溶液,产生沉淀,则CH3CH2Br在NaOH溶液中发生了水解 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
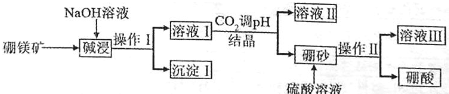
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
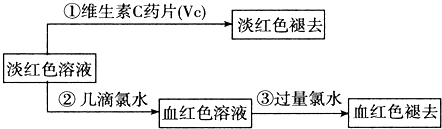
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com