
| ||
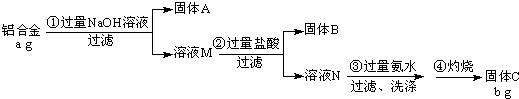
| ag |
| 9b |
| 17a |
| 9b |
| 17a |


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| Ԫ�ر�� | Ԫ�����ʻ�ṹ |
| T | M������2�ԳɶԵ��� |
| X | Ԫ�����������+7�� |
| Y | ��������Ԫ�صļ������а뾶��С |
| Z | ����������ɫ���塢���硢�ܶȱ�ˮС����ˮ���ҷ�Ӧ����������Ӧ��ͬ�����²��ﲻͬ |
| A�����Ӱ뾶��С�����˳��Y��Z��T��X |
| B��X��Y�γɻ�����ľ���������X��Z�γɻ�����ľ������Ͳ�ͬ |
| C��T���⻯����ͬ��Ԫ���⻯���зе���͵� |
| D��X������������Ӧ��ˮ���������������е���ǿ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
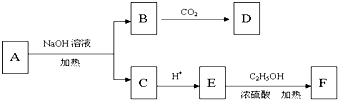
 ϩ��A��һ�������¿�����ͼ���з�Ӧ��
ϩ��A��һ�������¿�����ͼ���з�Ӧ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��ͼ��ʾˮ��Һ��c��H+����c��OH-���Ĺ�ϵ��
��ͼ��ʾˮ��Һ��c��H+����c��OH-���Ĺ�ϵ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��HCl��NaOH��Ӧ���к��ȡ�H=-57.3 kJ?mol-1����H2SO4��NaOH��Ӧ���к��ȡ�H=2����-57.3��kJ?mol-1 |
| B��CO��ȼ������283kJ?mol-1����2CO2��g��=2CO��g��+O2��g����H=2����+283��kJ?mol-1 |
| C��ͬ��ͬѹ�£�H2��g��+Cl2��g��=2HCl��g���ڹ��պ͵�ȼ�����·�Ӧ�ġ�H����ͬ |
| D����֪��2C��s��+2O2=2CO2��g����H1��2C��s��+O2=2CO��g����H2�����H1����H2 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com