
【题目】2015年斯坦福大学研究人员研制出一种可在一分钟内完成充放电的超常性能铝离子电池,内部用AlCl4﹣和有机阳离子构成电解质溶液,其放电工作原理如图所示.下列说法不正确的是( ) 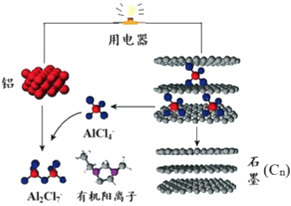
A.放电时,铝为负极、石墨为正极
B.放电时,有机阳离子向铝电极方向移动
C.放电时的负极反应为:Al﹣3e﹣+7AlCl4﹣═4Al2Cl7﹣
D.充电时的阳极反应为:Cn+AlCl4﹣﹣e﹣═CnAlCl4
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案 期末好成绩系列答案
期末好成绩系列答案科目:高中化学 来源: 题型:
【题目】标准状况下有①6.72L甲烷 ②3.01×1023个氯化氢分子 ③13.6g硫化氢④0.2mol NH3 . 下列对这四种气体的关系从小到大表示不正确的是( )
A.体积:④<①<②<③
B.密度:①<④<③<②
C.质量:④<①<③<②
D.氢原子数:②<④<③<①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下将1molCO 和3mol 水蒸气放在密闭的容器中发生下列反应CO(g)+H2O(g)CO2(g)+H2(g)达到平衡后,测得CO2为0.75mol,再通入6mol 水蒸气,达到新的平衡后,CO2和H2的物质的量之和为( )
A.1.2 mol
B.1.5 mol
C.1.8 mol
D.2.1 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据问题填空:
(1)配制一定物质的量浓度溶液时,会使所配溶液浓度偏高的是(填序号)
a.容量瓶在使用前内壁沾有水珠 b.定容时俯视读刻度
c.未冷却至室温就注入容量瓶并马上定容 d.向容量瓶转移液体时有少量流出
(2)容量瓶上标有(填序号)
①温度 ②浓度 ③容量 ④质量 ⑤刻度线 ⑥酸式或碱式
(3)将4g NaOH 固体溶解在10mL的水中,再稀释成1L,从中取出10mL,这10mL溶液的物质的量浓度是 .
(4)溶液、胶体和浊液这三种分散系的本质区别是(填序号),
A.是否是大量分子或离子的集合体 B.分散质粒子的大小
C.是否能通过滤纸 D.是否均一、透明、稳定
光束通过Fe(OH)3胶体时,可看到光亮的通路,这种现象叫 .
(5)实验室制取氯气的反应方程式是:MnO2+4HCl(浓)=MnCl2+Cl2↑+2H2O,在此反应中,被氧化的元素是 , 还原产物是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】废旧印刷电路板的回收利用可实现资源再生,并减少污染.
(1)用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜.已知:
Cu(s)+2H+(aq)=Cu2+(aq)+H2(g)△H=+64.39kJmol﹣1
2H2O2(l)=2H2O(l)+O2(g)△H=﹣196.46kJmol﹣1
H2(g)+ ![]() O2(g)=H2O(l)△H=﹣285.84kJmol﹣1
O2(g)=H2O(l)△H=﹣285.84kJmol﹣1
在 H2SO4溶液中Cu与H2O2反应生成Cu2+和H2O的热化学方程式为 .
(2)控制其他条件相同,印刷电路板的金属粉末用10%H2O2和3.0mol/LH2SO4的混合溶液处理,测得不同温度下铜的平均溶解速率(见表).
温度(℃) | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
铜平均溶解速率 | 7.34 | 8.01 | 9.25 | 7.98 | 7.24 | 6.73 | 5.76 |
当温度高于40℃时,铜的平均溶解速率随着反应温度升高而下降,其主要原因是 .
(3)在提纯后的CuSO4溶液中加入一定量的Na2SO3和NaCl溶液,加热,生成CuCl沉淀.制备CuCl的离子方程式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求完成下列填空:
(1)已知在标准状况下的四种气体 ①8.96L CH4②3.01×1022个HCl分子 ③10.2克H2S④0.5molNH3用相应的序号填写下列空白:
体积最大的是;含氢原子数最多的是 .
(2)等物质的量的氧气与臭氧质量之比为 , 分子个数之比为 , 电子个数之比为 .
(3)某金属氯化物MCl3 26.7g,含有0.600mol Cl﹣ . 则金属M的摩尔质量为 .
(4)现有10克H218O中,中子数目为 .
(5)0.4mol NH3中所含氢原子数与g水所含氢原子数相等.
(6)0.5molSO2的质量是g,在标准状况下的体积为L;含有个氧原子.
(7)将标况下22.4L的HCl 溶于水配成200mL的溶液,所溶液的物质的量浓度为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气可用来消灭田鼠,为此将氯气通过软管灌入洞中,这是利用了氯气下列性质中的
①黄绿色 ②密度比空气大 ③有毒 ④较易液化 ⑤溶解于水
A.②③B.③④C.①②③D.③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮元素在海洋中的循环,是整个海洋生态系统的基础和关键.海洋中无机氮的循环过程可用如图表示. 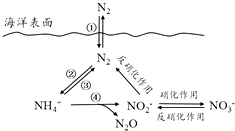
(1)海洋中的氮循环起始于氮的固定,其中属于固氮作用的一步是(填图中数字序号).
(2)下列关于海洋氮循环的说法正确的是(填字母序号).
a.海洋中存在游离态的氮
b.海洋中的氮循环起始于氮的氧化
c.海洋中的反硝化作用一定有氧气的参与
d.向海洋排放含NO3﹣的废水会影响海洋中NH4+的含量
(3)有氧时,在硝化细菌作用下,NH4+可实现过程④的转化,将过程④的离子方程式补充完整:
NH4++5O2═2NO2﹣+H+++
(4)有人研究了温度对海洋硝化细菌去除氨氮效果的影响,下表为对10L人工海水样本的监测数据:
温度/℃ | 样本氨氮含量/mg | 处理24h | 处理48h |
氨氮含量/mg | 氨氮含量/mg | ||
20 | 1008 | 838 | 788 |
25 | 1008 | 757 | 468 |
30 | 1008 | 798 | 600 |
40 | 1008 | 977 | 910 |
硝化细菌去除氨氮的最佳反应温度是 , 在最佳反应温度时,48h内去除氨氮反应的平均速率是mgL﹣1h﹣1 .
(5)为了避免含氮废水对海洋氮循环系统的影响,需经处理后排放.图是间接氧化工业废水中氨氮(NH4+)的示意图. 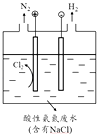
①结合电极反应式简述间接氧化法去除氨氮的原理: .
②若生成H2和N2的物质的量之比为3:1,则处理后废水的pH将(填“增大”、“不变”或“减小”),请简述理由: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了确定乙醇分子的结构简式是CH3—O—CH3还是CH3CH2OH,实验室利用如图所示的实验装置,测定乙醇与钠反应(ΔH<0)生成氢气的体积,并据此计算乙醇分子中能与金属钠反应的氢原子的数目。试回答下列问题: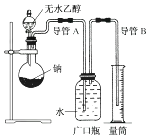
(1)指出实验装置中的错误:。
(2)若实验中用含有少量水的乙醇代替相同质量的无水乙醇,相同条件下,测得的氢气体积将(填“偏大”“偏小”或“不变”)。
(3)请指出能使该实验安全、顺利进行的关键实验步骤(至少指出两个关键步骤)
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com