
| A. | 正极反应:O2+2H2O+4e-═4OH- | |
| B. | 当正极消耗22.4 L H2时,负极11.2 L O2消耗(相同条件) | |
| C. | 发生氧化反应的是负极 | |
| D. | 氢氧燃料电池不仅能量转化率高,而且产物是水,属于环境友好电池 |
分析 根据电极反应式知,氢氧燃料碱性电池中,通入氢气的电极是负极,该极上发生氧化反应,通入氧气的电极是正极,该极上是氧气发生得电子的还原反应,电池反应式为2H2+O2=2H2O,燃烧产物是水,环保无污染.
解答 解:A、氢氧燃料碱性电池中,通入氧气的电极是正极,该极上是氧气发生得电子的还原反应,正极反应:O2+2H2O+4e-═4OH-,故A正确;
B、正极反应:O2+2H2O+4e-═4OH-,在正极上消耗的是氧气,负极上消耗的是氢气,故B错误;
C、氢氧燃料碱性电池中,通入氢气的电极是负极,该极上发生氧化反应,故C正确;
D、在燃料电池工作时,化学能大多数转化为电能,能量转化率高,并且2H2+O2=2H2O知,氢氧燃料电池的产物是水,水对环境没有污染,所以属于环境友好电池,故D正确.
故选B.
点评 本题考查原电池的组成以及工作原理,题目难度不大,注意电极反应式以及能量的转换形式,注意燃料电池中燃料不燃烧,为易错点.


科目:高中化学 来源: 题型:解答题
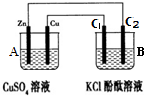 思考下列问题,按要求填空:
思考下列问题,按要求填空:| 加入的物质 | 少量(NH4)2SO4固体 | 少量HNO3溶液 | 少量KOH溶液 |
| c(OH-)的变化 | 减小 | 减小 | 增大 |
| 平衡移动方向 | 逆向 | 正向 | 逆向 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量悬浊液,过滤,充分洗涤后,取滤渣于试管中,加入过量2mol.L-1HCl,充分振荡,再加0.1mol.L-1BaCl2溶液 | 说明悬浊液中混有白色沉淀产生,有Cu4(0H)6S04. |
| 步骤2:另取少量悬浊液于试管中将试管放入装有沸水的小烧杯中,用水浴加热一段时间,取出试管观察 | 试管中黑色沉淀生成,说明悬浊液中混有Cu(0H)2. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | CaF2 | B. | CO2 | C. | NaCl | D. | CsCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ba2+、SO42-、SO32- | B. | Na+、C1-、OH- | ||
| C. | NH4+、OH -、SO42- | D. | H+、CO32-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molSiO2晶体内含有2NA个Si-O键 | |
| B. | 在0.1mol熔融KHSO4中,含有0.1NA个SO42- | |
| C. | 在0.5L 1mol•L-1的盐酸中所含粒子总数为NA | |
| D. | 1molSi晶体内含有2NA个Si-Si键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com