
分析 处于最低能量的原子叫做基态原子,基态电子排布遵循能量最低原理、保里不相容原理和洪特规则,根据元素符号,判断元素原子的核外电子数,再根据核外电子排布规律来写,以此解答该题.
解答 解:①自然界中含量居第二的金属元素为铁,电子排布式为1s22s22p63s23p63d64s2,故答案为:1s22s22p63s23p63d64s2;
②第四周期0族元素为Kr,电子排布式为1s22s22p63s23p63d104s24p6,故答案为:1s22s22p63s23p63d104s24p6;
③能形成自然界中最硬的单质的元素为碳,电子排布式为1s22s22p2,故答案为:1s22s22p2.
点评 本题考查了基态原子的核外电子排布式,根据核外电子排布规律来写,注意电子处于全满、半满、全空时最稳定,题目难度不大.


 快捷英语周周练系列答案
快捷英语周周练系列答案科目:高中化学 来源: 题型:选择题
| A. | 中和反应是吸热反应 | |
| B. | 需要加热的反应都是吸热反应 | |
| C. | 断裂化学键要吸收能量 | |
| D. | 反应物总能量一定等于生成物总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
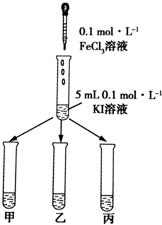 某学习小组通过下面的实验一和实验二,探究某些化学理论.
某学习小组通过下面的实验一和实验二,探究某些化学理论.| 序号 | 反应温度/℃ | C(HCl)/mol•L-1 | V(HCl)/ml | 10g碳酸钙的形状 | t/min |
| ① | 20 | 2 | 10 | 块状 | t 1 |
| ② | 20 | 4 | 10 | 块状 | t 2 |
| ③ | 20 | 2 | 10 | 粉末 | t 3 |
| ④ | 40 | 2 | 10 | 粉末 | t 4 |
| ⑤ | 40 | 4 | 10 | 粉末 | t5 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
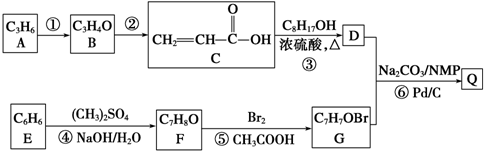
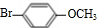 .
.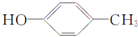 .
. +
+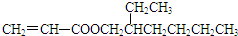 $→_{Na_{2}CO_{3}/NMP}^{Pd/C}$
$→_{Na_{2}CO_{3}/NMP}^{Pd/C}$ 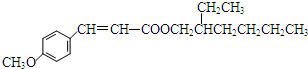 +HBr.
+HBr.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:C、Al、K依次增大 | |
| B. | 热稳定性:HF、NH3、SiH4依次增大 | |
| C. | 水化物的酸碱性:NaOH、Al(OH)3、Mg(OH)2碱性减弱 | |
| D. | 非金属性:Cl、P、S依次增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 检验蔗糖是否水解:蔗糖溶液在稀硫酸存在下水浴加热一段时间后,再与银氨溶液混合加热,观察现象 | |
| B. | 检验溶液中是否含有NH4+:取少量待检溶液,向其中加入浓NaOH溶液加热,再用湿润的蓝色石蕊试纸放置试管口,观察现象 | |
| C. | 提纯含有少量苯酚的苯:向含有少量的苯酚的苯中加入过量的浓溴水,震荡后静置过滤,除去三溴苯酚沉淀 | |
| D. | 除去淀粉溶液中的氯化钠:用蒸馏水渗析法 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4 (g)+2O2(g)═CO2 (g)+2H2O(l)△H=a kJ•mol-1 CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=b kJ•mol-1 | |
| B. | 2H2(g)+O2(g)═2H2O(l)△H=a kJ•mol-1 H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=b kJ•mol-1 | |
| C. | C(s)+$\frac{1}{2}$O2 (g)═CO(g)△H=a kJ•mol-1 C(s)+O2(g)═CO2(g)△H=b kJ•mol-1 | |
| D. | S(g)+O2(g)═SO2 (g)△H=a kJ•mol-1 S(s)+O2(g)═SO2(g)△H=b kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气溶于水后得到的溶液叫做氯水或液氯 | |
| B. | 次氯酸不稳定,见光易分解出氯气 | |
| C. | 反应Cl2+H2O=HCl+HClO中,H2O是还原剂 | |
| D. | 漂白粉属于混合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com