
| A.Mg2+、NH4+、Cl—、OH— | B.Na+、AlO2—、CO32—、OH— |
| C.Ca2+、Fe3+、H+、NO3— | D.Fe3+、K+、SCN—、SO42— |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:单选题
| A.Na+、H+、CO32-、Cl- | B.Na+、Ba2+、Cl-、SO42- |
| C.K+、 H+、SO42-、OH- | D.Ag+、Al3+、NO3-、H+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在含有大量I-离子的溶液中:Cl¯、Fe3+、Al3+、Cu2+ |
| B.滴加石蕊试液显红色的溶液:Fe2+、NH4+、Cl-、NO3-能够大量共存 |
| C.在由水电离出的c(H+)=10-12 mol·L-1的溶液中:Na+、Ba2+、Cl¯、Br¯ |
| D.在加入Al能放出大量H2的溶液中:NH4+、SO42¯、C1¯、HCO3¯ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Na+I- CO32- ClO- | B.Fe2+ H+K+NO3- |
| C.Cu2+ Fe2+Cl- NO3- | D.Ba2+Na+ SCN- Cl- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
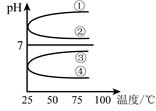
 ; ②
; ②  ;
;
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Na+、Cu2+、NO3-、CO32- | B.Cu2+、K+、Cl-、SO32- |
| C.Fe2+、Na+、SO42-、NO3- | D.Mg2+、NH4+、SO42-、Cl- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Al3+、CH3COO—、Cl— | B.Mg2+、Ba2+、Br— |
| C.Mg2+、Cl—、I— | D.Na+、NH4+、Cl— |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 弱酸 | CH3COOH | H2SO3 | HCN |
| 物质的量浓度mol/L | 0.01 | 0.01 | 0.01 |
| PH | 3.4 | 2.3 | 5.6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com