
【题目】下列反应既属于非氧化还原反应,又是放热反应的是( )
A.锌粒与稀硫酸的反应
B.酸碱中和反应
C.甲烷在氧气中的燃烧反应
D.Ba(OH)2·8H2O晶体与NH4Cl晶体的反应
科目:高中化学 来源: 题型:
【题目】下列描述中正确的是( )
A.CS2为V形的极性分子
B.ClO3﹣的空间构型为平面三角形
C.SiF4和SO32﹣的中心原子均为sp2杂化
D.SF6中有6对相同的成键电子对
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把碎纸片b补充到a中,可得到一个完整的离子方程式(未配平)。下列说法正确的是( )

A. 反应物微粒是S、SO![]() 、OH-
、OH-
B. 该反应可能在酸性条件下进行
C. 氧化剂与还原剂的物质的量之比为2∶1
D. 2 mol S参加反应时,转移的电子数为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气是一种有毒气体,在运输和储存过程中必须防止泄露。若储存液氯的钢瓶发生泄露,立即采取的措施中错误的是()
A.用浸有水的毛巾捂住口鼻B.将人群逆风向疏散
C.将人群向低处疏散D.向泄露地点撒一些石灰
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物X是合成二氢荆芥内酯的重要原料,其结构简式为 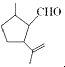 ,下列检验X中既含碳碳双键又含醛基的试剂和顺序正确的是( )
,下列检验X中既含碳碳双键又含醛基的试剂和顺序正确的是( )
A.先加酸性高锰酸钾溶液,后加银氨溶液,加热
B.先加溴水,后加酸性高锰酸钾溶液
C.先加银氨溶液,加热,再加入溴水
D.先加入新制氢氧化铜悬浊液,加热,取清液酸化后再加溴水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图中X、Y为单质,其他为化合物,它们之间存在如下转化关系(部分产物已略去)。其中,A俗称磁性氧化铁。
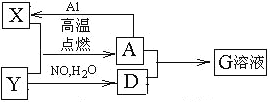
回答下列问题:
(1)NaOH中存在的化学键的类型为_____________。
(2)写出Y![]() D 的化学方程式:________________。
D 的化学方程式:________________。
(3)写出A和D的稀溶液反应生成G的离子方程式:________________。
(4)向含4mol D的稀溶液中,逐渐加入X粉末至过量,假设生成的气体只有一种,请在坐标系中画出n(X2+)随n(X)变化的示意图,并标出n(X2+)的最大值_______。
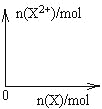
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在CO2中,Mg燃烧生成MgO和C.下列说法正确的是( )
A.元素C的单质只存在金刚石和石墨两种同素异形体
B.Mg、MgO中镁元素微粒的半径:r(Mg2+)>r(Mg)
C.在该反应条件下,Mg的还原性强于C的还原性
D.该反应中化学能全部转化为热能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业合成氨的反应如下:N2(g)+3H2(g)2NG3(g). 某温度下,在容积恒定为2.0L的密闭容器中充入2.0molN2和2.0molH2 , 一段时间后反应达平衡状态,实验数据如下表所示:
t/s | 0 | 50 | 150 | 250 | 350 |
n(NH3) | 0 | 0.24 | 0.36 | 0.40 | 0.40 |
(1)0~50s内的平均反应速率 v(N2)= .
(2)250s时,H2的转化率为
(3)已知N≡N的键能为946kJ/mol,H﹣H的键能为436kJ/mol,N﹣H的键能为391kJ/mol,则生成1molNH3过程中的热量变化kJ.下图能正确表示该反应中能量变化的是 . 
(4)为加快反应速率,可以采取的措施 a.降低温度 b.增大压强 c.恒容时充入He气d.恒压时充入He气 e.及时分离NH3
(5)下列说法错误的是 a.使用催化剂是为了加快反应速率,提高生产效率
b.上述条件下,N2不可能100%转化为NH3
c.为了提高N2的转化率,应适当提高H2的浓度
d.250~350s生成物浓度保持不变,反应停止.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有前四周期的5种元素的部分信息如下表所示:
元素代号 | 元素部分信息 |
X | X的阴离子核外电于云均呈球形 |
Y | 原子的能级上有3个未成对电子,其最简单气态氢化物在水中的溶解度在同族元素所形成的最简单气态氢化物中最大 |
Z | 基态原于核外有3个能级填充了电子,能量最高能级的电子数等于前两个能级的电子数之和 |
R | 元素原于的围电子排布式为nsn-1npn-1 |
T | 一种核素的质量数为65,中子数为36 |
根据上述元素信息,回答下列问题:
(1)基态T2+的电子排布式为____________。
(2)Y.Z.R 的电负性由大到小的顺序为____________ (用元素符号表示)。
(3)YX4+的空间构型为____________,离子中Y原子的杂化轨道类型为____________ ,YX4+电子式为________。
(4)YX3的一种等电子体分子是______,YX3 的键角大于X2Z的键角的主要原因是________。
(5)T单质不溶于YX3溶液,也不溶于X2Z溶液,但能溶于它们的混合溶液,其主要原因是形成了稳定的[T(YX3)4]2+,1mol该阳离子中共含有______mol σ键。
(6)Z、T组成的晶胞结构如下图所示。已知Z、T原子的半径分别为apm、bpm,晶胞边长为cpm,则该晶胞中原子的空间利用率为________(用代数式表示)。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com