
ΓΨΧβΡΩΓΩ“―÷ΣΥ°‘Ύ25ΓφΚΆ95Γφ ±Θ§ΒγάκΤΫΚβ«ζœΏ»γΆΦΥυ ΨΘΚ 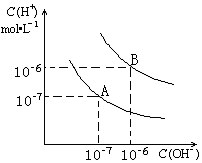
Θ®1Θ©‘ρ25Γφ ±Υ°ΒΡΒγάκΤΫΚβ«ζœΏ”ΠΈΣΘ®ΧνΓΑAΓ±ΜρΓΑBΓ±Θ©Θ§«κΥΒΟςάμ”…
Θ®2Θ©25Γφ ±Θ§ΫΪpH=9ΒΡNaOH»ή“Κ”κpH=4ΒΡH2SO4»ή“ΚΜλΚœΘ§»τΥυΒΟΜλΚœ»ή“ΚΒΡ pH=7Θ§‘ρNaOH»ή“Κ”κH2SO4»ή“ΚΒΡΧεΜΐ±»ΈΣ
Θ®3Θ©95Γφ ±Θ§»τ100ΧεΜΐpH1=aΒΡΡ≥«ΩΥα»ή“Κ”κ1ΧεΜΐpH2=bΒΡΡ≥«ΩΦν»ή“ΚΜλΚœΚσ»ή“Κ≥ ÷––‘Θ§‘ρΜλΚœ«ΑΘ§ΗΟ«ΩΥαΒΡpH1”κ«ΩΦνΒΡpH2÷°Φδ”Π¬ζΉψΒΡΙΊœΒ «
Θ®4Θ©«ζœΏBΕ‘”ΠΈ¬Ε»œ¬Θ§pH=2ΒΡΡ≥HA»ή“ΚΚΆpH=10ΒΡNaOH»ή“ΚΒ»ΧεΜΐΜλΚœΚσΘ§ΜλΚœ»ή“ΚΒΡpH=5Θ°«κΖ÷ΈωΤδ‘≠“ρΘΚ Θ°
ΓΨ¥πΑΗΓΩ
Θ®1Θ©AΘΜΥ°ΒΡΒγάκ ±Έϋ»»Ιΐ≥Χ,Φ”»»¥ΌΫχΒγάκ,Έ¬Ε»ΒΆ,Υ°ΒΡάκΉ”Μΐ–Γ
Θ®2Θ©10ΘΚ1
Θ®3Θ©pH1+pH2=14,Μρa+b=14
Θ®4Θ©«ζœΏBΕ‘”Π95Γφ,¥Υ ±Υ°ΒΡάκΉ”ΜΐΈΣ10©¹12,HAΈΣ»θΥα,HA÷–ΚΆNaOHΚσ,ΜλΚœ»ή“Κ÷–ΜΙ Θ”ύΫœΕύΒΡHAΖ÷Ή”,Ω…ΦΧ–χΒγάκ≥ωH+, Ι»ή“ΚpH=5
ΓΨΫβΈωΓΩΫβΘΚΘ®1Θ©«ζœΏAΧθΦΰœ¬Kw=cΘ®H+Θ©ΓΝcΘ®OH©¹Θ©=10©¹7ΓΝ10©¹7=10©¹14Θ§«ζœΏBΧθΦΰœ¬cΘ®H+Θ©=cΘ®OH©¹Θ©=10©¹6 mol/LΘ§Kw=cΘ®H+Θ©cΘ®OH©¹Θ©=10©¹12 ΘΜΥ°ΒΡΒγάκ ±Έϋ»»Ιΐ≥ΧΘ§Φ”»»¥ΌΫχΒγάκΘ§Υυ“‘A«ζœΏ¥ζ±μ25Γφ ±Υ°ΒΡΒγάκΤΫΚβ«ζœΏΘ§
Ι ¥πΑΗΈΣΘΚAΘΜΥ°ΒΡΒγάκ ±Έϋ»»Ιΐ≥ΧΘ§Φ”»»¥ΌΫχΒγάκΘ§Έ¬Ε»ΒΆΘ§Υ°ΒΡάκΉ”Μΐ–ΓΘΜΘ®2Θ©25Γφ ±ΥυΒΟΜλΚœ»ή“ΚΒΡpH=7Θ§»ή“Κ≥ ÷––‘Φ¥ΥαΦν«ΓΚΟ÷–ΚΆΘ§Φ¥nΘ®OH©¹Θ©=nΘ®H+Θ©Θ§‘ρVΘ®NaOHΘ©10©¹5 molL©¹1=VΘ®H2SO4Θ©10©¹4 molL©¹1Θ§ΒΟVΘ®NaOHΘ©ΘΚVΘ®H2SO4Θ©=10ΘΚ1Θ§Ι ¥πΑΗΈΣΘΚ10ΘΚ1ΘΜΘ®3Θ©“ΣΉΔ“βΒΡ «95ΓψC ±Θ§Υ°ΒΡάκΉ”ΜΐΈΣ10©¹12Θ§Φ¥ΥαΓΔΦν≈®Ε»œύΒ» ±pHΘ®ΥαΘ©+pHΘ®ΦνΘ©=12Θ°œ÷«ΩΦνΒΡOH©¹≈®Ε» ««ΩΥαH+≈®Ε»ΒΡ100±ΕΘ§Υυ“‘pHΘ®ΥαΘ©+pHΘ®ΦνΘ©=14Θ§Φ¥pH1+pH2=14Θ§Μρa+b=14Θ§Ι ¥πΑΗΈΣΘΚpH1+pH2=14Θ§Μρa+b=14ΘΜΘ®4Θ©‘Ύ«ζœΏBΕ‘”ΠΈ¬Ε»œ¬Θ§“ρpHΘ®ΥαΘ©+pHΘ®ΦνΘ©=12Θ§Ω…ΒΟΥαΦνΝΫ»ή“Κ÷–cΘ®H+Θ©=cΘ®OH©¹Θ©Θ§»γ ««ΩΥαΦνΘ§ΝΫ»ή“ΚΒ»ΧεΜΐΜλΚœΚσ»ή“Κ≥ ÷––‘ΘΜœ÷ΜλΚœ»ή“ΚΒΡpH=5Θ§Φ¥Β»ΧεΜΐΜλΚœΚσ»ή“Κœ‘Υα–‘Θ§ΥΒΟςH+”κOH©¹Άξ»ΪΖ¥”ΠΚσ”÷”––¬ΒΡH+≤ζ…ζΘ§ΥαΙΐΝΩΘ§Υυ“‘ΥαHA «»θΥαΘ§
Ι ¥πΑΗΈΣΘΚ«ζœΏBΕ‘”Π95ΓφΘ§¥Υ ±Υ°ΒΡάκΉ”ΜΐΈΣ10©¹12Θ§HAΈΣ»θΥαΘ§HA÷–ΚΆNaOHΚσΘ§ΜλΚœ»ή“Κ÷–ΜΙ Θ”ύΫœΕύΒΡHAΖ÷Ή”Θ§Ω…ΦΧ–χΒγάκ≥ωH+Θ§ Ι»ή“ΚpH=5Θ°
Θ®1Θ©Κα÷α ««βάκΉ”≈®Ε»Θ§Ήί÷α ««β―θΗυάκΉ”≈®Ε»Θ§Υ°ΒΡάκΉ”Μΐ≥Θ ΐKw=cΘ®H+Θ©ΓΝcΘ®OH©¹Θ©ΦΤΥψ≥ωA«ζœΏΒΡKw÷ΒΫαΚœΥ°ΒΡΒγάκ ±Έϋ»»±»Ϋœ≈–Εœ25Γφ ±Υ°ΒΡΒγάκΤΫΚβ«ζœΏΘΜΘ®2Θ©ΗυΨί»ή“ΚΒΡpHΦΤΥψ≥ω»ή“Κ÷–«βάκΉ”ΓΔ«β―θΗυάκΉ”≈®Ε»Θ§‘ΌΝ– ΫΦΤΥψ≥ω«β―θΜ·ΡΤ»ή“ΚΚΆΝρΥα»ή“ΚΒΡΧεΜΐΘΜΘ®3Θ©ΥαΓΔΦνΕΦ ««ΩΒγΫβ÷ Θ§»ή“Κ≥ ÷––‘ΥΒΟς«βάκΉ”ΚΆ«β―θΗυάκΉ”ΒΡΈο÷ ΒΡΝΩœύΒ»Θ§ΫαΚœΥ°ΒΡάκΉ”Μΐ≥Θ ΐ»ΖΕ®«ΩΥαΒΡpH1”κ«ΩΦνΒΡpH2÷°Φδ”Π¬ζΉψΒΡΙΊœΒΘΜΘ®4Θ©ΗυΨί«ζœΏBΕ‘”ΠΈ¬Ε»œ¬pH=5Θ§ΥΒΟς»ή“Κœ‘ ΨΥα–‘Θ§Ζ¥”ΠΚσ«βάκΉ”ΙΐΝΩΖ÷ΈωΘ°


 –Γ―ßΫΧ≤ΡΆξ»ΪΫβΕΝœΒΝ–¥πΑΗ
–Γ―ßΫΧ≤ΡΆξ»ΪΫβΕΝœΒΝ–¥πΑΗ
| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΈΔΝΩ‘ΣΥΊ‘Ύ…ζΈοΧεΡΎΥδ»ΜΚή…ΌΘ§»¥ «Έ§≥÷…ζΟϋΜνΕ·≤ΜΩ…»±…ΌΒΡΘ§œ¬ΟφΡΡ“Μ Βάΐ÷ΛΟςΝΥ
A. Mg «“Ε¬ΧΥΊΒΡΉι≥…≥…Ζ÷
B. ”Ά≤Υ»±…ΌB ±÷ΜΩΣΜ®≤ΜΫαΙϊ
C. Ε·Έο―Σ“ΚCa―ΈΚ§ΝΩΧΪΒΆΘ§Μα≥ι¥Λ
D. »±PΜα”ΑœλΚΥΥαΒΡΚœ≥…
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–Μ·―ß”Ο”ο Ι”Ο’ΐ»ΖΒΡ «Θ® Θ©
A. ΤœΧ―Χ«Θ®C6H12O6Θ©ΓΔΒμΖέ[Θ®C6H10O5Θ©n]ΒΡΉνΦρ ΫΕΦ «CH2O
B. ““¥ΦΒΡΖ÷Ή” ΫΘΚC2H5OH
C. ““»©Ζ÷Ή”ΒΡΫαΙΙΦρ Ϋ «CH3COH
D. ±ϊœ©Ζ÷Ή”ΒΡ«ρΙςΡΘ–Ά «![]()
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–ΙΊ”ΎΜ·―ßΦϋΒΡΥΒΖ®’ΐ»ΖΒΡ «(ΓΓΓΓ)
A.ΙΙ≥…ΒΞ÷ Ζ÷Ή”ΒΡΈΔΝΘ“ΜΕ®Κ§”–Ι≤ΦέΦϋ
B.»Ϊ≤Ω”…Ζ«Ϋπ τ‘ΣΥΊΉι≥…ΒΡΜ·ΚœΈο÷–Ω…ΡήΚ§”–άκΉ”Φϋ
C.Ζ«ΦΪ–‘Φϋ÷Μ¥φ‘Ύ”ΎΖ«Ϋπ τΒΞ÷ ΜρΙ≤ΦέΜ·ΚœΈο÷–
D.Μ·―ßΦϋΑϋά®άκΉ”ΦϋΓΔΙ≤ΦέΦϋΓΔ«βΦϋ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–ΥΒΖ®’ΐ»ΖΒΡ «( )
A. ΦΉ±ΫΚΆ“ΚδεΙβ’’»Γ¥ζ≤ζΈοΈΣ![]()
B. ““±ΫΚΆ¬»ΤχΙβ’’…ζ≥…≤ζΈο”–11÷÷
C. Ζ÷Ή” ΫΈΣC5H10O2ΒΡΥυ”–θΞάύΒΡΆ§Ζ÷“λΙΙΧεΙ≤Θ®≤ΜΚ§ΝΔΧε“λΙΙΘ©7÷÷
D. 2-¬»-2-ΕΓœ©≤Μ¥φ‘ΎΥ≥Ζ¥“λΙΙ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ”ΟΟΨ“Μ¥Έ¬»ΥαΡΤ»ΦΝœΒγ≥ΊΉςΒγ‘¥ΡΘΡβœϊ≥ΐΙΛ“ΒΥα–‘ΖœΥ°÷–ΒΡCr2O72-ΒΡΙΐ≥Χ(ΫΪΓΑCr2O72-Γ±ΜΙ‘≠ΈΣΓΑCr3+Γ±)Θ§ΉΑ÷Ο»γΆΦΥυ ΨΓΘœ¬Ν–ΥΒΖ®÷–¥μΈσΒΡ «
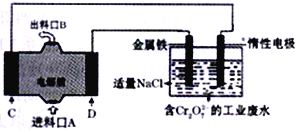
A. Ϋπ τΧζΒγΦΪΒΡΖ¥”ΠΈΣ:Fe-2e-=Fe2+
B. ΉΑ÷Ο÷–ΒγΉ”ΒΡΝςΕ·¬ΖœΏ «: CΒγΦΪΓζΕη–‘ΒγΦΪΓζΫπ τΧζΒγΦΪΓζDΒγΦΪ
C. ΉΑ÷ΟΙΛΉςΙΐ≥Χ÷–œϊΚΡ14.4gMgΘ§άμ¬έ…œΩ…œϊ≥ΐCr2O72-0.1mol
D. ΫΪCr2O72-¥ΠάμΚσΒΡΖœΥ°±»‘≠ΙΛ“ΒΖœΥ°ΒΡpH‘ω¥σ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ25Γφ ±Θ§‘Ύ20ml 0.1molL©¹1NaOH»ή“Κ÷–÷πΒΈΦ”»κ0.2molL©¹1¥ΉΥα»ή“ΚΘ§ΒΈΕ®«ζœΏ»γΆΦΥυ ΨΘ§”–ΙΊΝΘΉ”≈®Ε»ΒΡΙΊœΒ÷–Θ§≤Μ’ΐ»ΖΒΡ «Θ®ΓΓΓΓΘ© 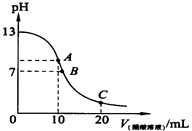
A.‘ΎAΒψΘΚcΘ®Na+Θ©ΘΨcΘ®OH©¹Θ©ΘΨcΘ®CH3COO©¹Θ©ΘΨcΘ®H+Θ©
B.‘ΎBΒψΘΚcΘ®Na+Θ©©³cΘ®CH3COO©¹Θ©ΘΨcΘ®OH©¹Θ©©³cΘ®H+Θ©
C.‘ΎCΒψΘΚcΘ®CH3COO©¹Θ©ΘΨcΘ®Na+Θ©ΘΨcΘ®H+Θ©ΘΨcΘ®OH©¹Θ©
D.‘ΎCΒψΘΚcΘ®CH3COO©¹Θ©+cΘ®CH3COOHΘ©©³2 cΘ®Na+Θ©
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–Ηςœν÷–Θ§≤Μ τ”Ύ÷§άύΈο÷ ΒΡ «Θ® Θ©
A. Έ§…ζΥΊD B. Β®ΙΧ¥Φ C. –έ–‘ΦΛΥΊ D. ÷§ΖΨΟΗ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ…ζΈοœΗΑϊ÷–Κ§ΝΩΉνΕύΒΡΝΫ÷÷Μ·ΚœΈοΥυΙ≤”–ΒΡ‘ΣΥΊ «
A. CΓΔHΓΔOΓΔN B. CΓΔHΓΔO C. HΓΔO D. N
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΑΌΕ»÷¬–≈ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com