
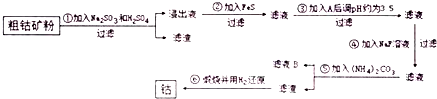
分析 粗钴矿粉主要含Co2O3、CuO、Fe2O3、CaO、MgO、SiO2等,其中Co2O3不能完全溶于硫酸,而CoO溶于硫酸.粗钴矿粉中加入硫酸溶解生成Co2(SO4)3、硫酸铜、硫酸铁、硫酸钙、硫酸镁,再加入亚硫酸钠溶液,可以还原三价钴离子、铁离子为二价钴离子和亚铁离子,过滤得到滤渣为二氧化硅,浸出液中加入FeS实现程度转化完全沉淀铜离子生成CuS沉淀,已知:H2O2、Cl2均不能氧化Co2+,过滤得到滤液中加入氧化剂过氧化氢或氯气氧化亚铁离子为铁离子,调节溶液PH=3.5铁离子全部沉淀,过滤得到滤液中加入NaF溶液沉淀镁离子和钙离子,过滤得到滤液中加入碳酸铵溶液沉淀二价钴离子生成CoCO3沉淀,滤液中主要是铵盐溶液,滤渣为CoCO3沉淀,煅烧得到CoO,用氢气还原得到金属钴;
(1)步骤①所得滤渣为二氧化硅,还需加入Na2SO3的原因是还原三价钴离子,铁离子;
(2)步骤②加入FeS是为了除去Cu2+,发生沉淀转化生成CuS沉淀,步骤④所发生反应是氟离子沉淀钙离子和镁离子生成沉淀除去;
(3)步骤③加入A试剂从环保的角度考虑应是过氧化氢,调pH的目的是沉淀铁离子;
(4)滤液B中的阳离子为铵根离子,依据铵根离子和氢氧根离子反应生成氨气,利用湿润的红色石蕊试纸检验氨气的存在设计实验;
(5)依据反应中H2+CoO$\frac{\underline{\;\;△\;\;}}{\;}$Co+H2O,氧化还原反应电子转移总数和反应定量关系计算钴元素质量,得到样品中钴的质量分数.
解答 解:由流程可知,粗钴矿粉主要含Co2O3、CuO、Fe2O3、CaO、MgO、SiO2等,其中Co2O3不能完全溶于硫酸,而CoO溶于硫酸.粗钴矿粉中加入硫酸溶解生成Co2(SO4)3、硫酸铜、硫酸铁、硫酸钙、硫酸镁,再加入亚硫酸钠溶液,可以还原三价钴离子、铁离子为二价钴离子和亚铁离子,过滤得到滤渣为二氧化硅,浸出液中加入FeS实现程度转化完全沉淀铜离子生成CuS沉淀,已知:H2O2、Cl2均不能氧化Co2+,过滤得到滤液中加入氧化剂过氧化氢或氯气氧化亚铁离子为铁离子,调节溶液PH=3.5铁离子全部沉淀,过滤得到滤液中加入NaF溶液沉淀镁离子和钙离子,过滤得到滤液中加入碳酸铵溶液沉淀二价钴离子生成CoCO3沉淀,滤液中主要是铵盐溶液,滤渣为CoCO3沉淀,煅烧得到CoO,用氢气还原得到金属钴;
(1)步骤①所得滤渣为二氧化硅,化学式为SiO2,还需加入Na2SO3的原因是还原三价钴离子,铁离子,还原三价钴离子反应的离子方程式为:2Co3++SO32-+H2O=2Co2++2H++SO42-;
故答案为:SiO2;2Co3++SO32-+H2O=2Co2++2H++SO42-;
(2)步骤②加入FeS是为了除去Cu2+,发生沉淀转化生成CuS沉淀,反应的离子方程式为:FeS+Cu2+=CuS+Fe2+;步骤④所发生反应是氟离子沉淀钙离子和镁离子生成沉淀除去,反应的离子方程式为:Ca2++2F-=CaF2↓、Mg2++2F-=MgF2↓;
故答案为:FeS+Cu2+=CuS+Fe2+;Ca2++2F-=CaF2↓、Mg2++2F-=MgF2↓;
(3)步骤③加入A试剂从环保的角度考虑应是过氧化氢,过氧化氢做氧化剂被还原生成水,无其他杂质引入,调pH的目的是沉淀铁离子;
故答案为:H2O2;沉淀铁离子;
(4)滤液B中的阳离子为铵根离子,依据铵根离子和氢氧根离子反应生成氨气,利用湿润的红色石蕊试纸检验氨气的存在设计实验,具体步骤和现象为:取滤液少许加入试管中,加入氢氧化钠溶液加热,用湿润的红色石蕊试纸靠近试管口,若变蓝色证明生成了氨气,原滤液中含有NH4+;
故答案为:取滤液少许加入试管中,加入氢氧化钠溶液加热,用湿润的红色石蕊试纸靠近试管口,若变蓝色证明生成了氨气,原滤液中含有NH4+;
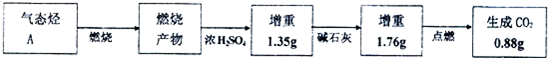
(5)H2+CoO$\frac{\underline{\;\;△\;\;}}{\;}$Co+H2O,反应中电子转移总数为2e-,转移2mol电子生成Co为1mol,则最后用H2还原时转移的电子数为0.1mol,生成Co物质的量为0.05mol,整个过程钴元素未损失,得到样品中钴的质量分数=$\frac{0.05mol×59g/mol}{20.00g}$×100%=14.75%,
故答案为:14.75%.
点评 本题考查了物质制备的工业流程分析判断,试剂选择的原则和方法,除杂的步骤分析应用,主要是题干信息理解和物质性质的应用判断,掌握基础是关键,题目难度中等.


 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 治理“地沟油”,可通过水解反应制得肥皂 | |
| B. | 硅晶体具有半导体性能,可用于制取光导纤维 | |
| C. | 人类超量碳排放及氮氧化物和二氧化硫的排放是形成酸雨的主要原因 | |
| D. | PM2.5是指空气中直径≤2.5 μm的颗粒物,直径为2.5 μm的颗粒物分散在空气中形成胶体(1μm=10-6m) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe3O4溶于足量稀HNO3:Fe3O4+8H+=Fe2++2Fe3++4H2O | |
| B. | 硅酸钠溶液与醋酸溶液混合:SiO32-+2H+=H2SiO3↓ | |
| C. | AlCl3溶液中加入过量的氨水:Al3++4OH-=AlO2-+2H2O | |
| D. | 向NaHCO3溶液中加入过量Ca(OH)2溶液:HCO3-+Ca2++OH-=CaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 食盐可作调味剂,也可作食品防腐剂 | |
| B. | 小苏打是一种膨松剂,可用于制作馒头和面包 | |
| C. | 煤经过气化和液化等物理变化可以转化为清洁燃料 | |
| D. | 次氯酸钠溶液可用于环境的消毒杀菌 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 对太阳光进行光谱分析,可证明太阳上是否含有Ar元素 | |
| B. | 利用焰色反应鉴别NaCl和KCl两种溶液 | |
| C. | 利用石灰水鉴别纯碱和小苏打两种溶液 | |
| D. | 利用烧碱溶液鉴别MgCl2和AlCl3两种溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | ②③ | C. | ②④ | D. | ③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com