
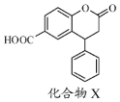
| A. | 分子中两个苯环一定处于同一平面 | |
| B. | 不能与饱和Na2CO3溶液反应 | |
| C. | 1 mol化合物X最多能与2 molNaOH反应 | |
| D. | 在酸性条件下水解,水解产物只有一种 |
分析 有物含有酯,可生水解反,含有基,具有酸,可生中和、酯化反应,结合有物结构特点解答题.
解答 解:A.两苯环连接在饱和原子上具有甲烷结构点且-C为键可自由旋,则分子中两个苯不一定处于同一平面,故A错误;
B.含有羧基,具有酸性,可与碳酸钠溶液反应,故B错误;
C.含有酯基,且可水解生成酚羟基和羧基,都可与氢氧化钠反应,且含有羧基,则1 mol化合物X最多能与3 molNaOH反应,故C错误;
D.能水解的只有酯基,且为环状化合物,则水解产物只有一种,故D正确.
故选D.
点评 本题查有机物的结构与性,为高频考点,题目中等,注意把握官能团的性质,为解答该题的关键,题目有利于培养学生良好的科学素养,提高分析能力,


 寒假学与练系列答案
寒假学与练系列答案科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
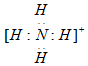 .写出实验室检验溶液中该离子的简单实验方案:取适量待测液于试管中,加入适量NaOH溶液后加热,若产生无色有刺激性气味的气体,且能使试管口湿润的红色石蕊试纸变蓝,则证明溶液中含有铵根离子.
.写出实验室检验溶液中该离子的简单实验方案:取适量待测液于试管中,加入适量NaOH溶液后加热,若产生无色有刺激性气味的气体,且能使试管口湿润的红色石蕊试纸变蓝,则证明溶液中含有铵根离子.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
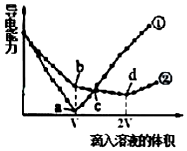 镁、钡是位于同一主族的活泼的金属元素.
镁、钡是位于同一主族的活泼的金属元素. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使用铁触媒,加快合成氨反应速率 | |
| B. | 乙酸乙酯在碱性条件下水解比在酸性条件下水解更有利 | |
| C. | 打开汽水瓶盖,即有大量气泡逸出 | |
| D. | 配置FeCl3溶液时,加入少量盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+ | B. | HSO3- | C. | AlO2- | D. | Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 ,有关该化合物的下列说法错误的是( )
,有关该化合物的下列说法错误的是( )| A. | 分子式为C12H18O2 | |
| B. | 分子中至少有6个碳原子共平面 | |
| C. | 该化合物能使酸性高锰酸钾褪色 | |
| D. | 一定条件下,1mol该化合物最多可与3mol H2加成 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com