
| A. | 常温下,78g Na202中含有的阴离子数为2NA | |
| B. | 常温下,1L 0.1 mol/L NH4NO3溶液中含有的NH4 +数为0.1NA | |
| C. | 标准状况下,22.4 L己烷中含有的共价键的数目为19 NA | |
| D. | 30 g SiO2晶体中含有Si-O键的数目为2 Na |
分析 A、根据过氧化钠的物质的量结合一个过氧化钠化学式中含有的阴离子个数计算总阴离子个数;
B、铵根离子水解导致铵根离子小于0.1mol;
C、标准状况下己烷不是气体;
D、1molSiO2晶体存在4molSi-O键;
解答 解:A.常温下,78g Na202的物质的量是n=$\frac{m}{M}$=$\frac{78g}{78g/mol}$=1mol,一个过氧化钠化学式中含有1个阴离子,78gNa2O2的物质的量是1mol,所以含有的阴离子数是1×6.02×1023,故A错误;
B、铵根离子水解导致铵根离子小于0.1mol,所以铵根离子的个数小于0.1NA,故B错误;
C、标准状况下己烷不是气体,不能使用标况下的气体摩尔体积计算22.4L己烷的物质的量,故C错误;
D、1molSiO2晶体存在4molSi-O键,所以30gSiO2晶体物质的量=$\frac{30g}{60g/mol}$=0.5mol,即0.5mol含有2molSi-O键,含有Si-O键的数目为2 NA ,故B正确;
故选D.
点评 本题主要考查了阿伏加德罗常数的分析判断,主要是二氧化硅晶体结构,气体摩尔体积应用条件,盐类水解分析,难度不大,掌握原子晶体的结构是解题的关键.


科目:高中化学 来源: 题型:选择题
| A. | Na投入水中:Na+H2O═Na++OH-+H2↑ | |
| B. | NaHCO3溶液与氢氧化钠溶液反应:HCO3-+2OH-═CO2↑+H2O | |
| C. | 用CH3COOH 溶液CaCO3:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| D. | 向NaAlO2溶液中通入过量CO2制Al(OH)3:CO2+AlO2-+2H20═Al(OH)3↓+HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
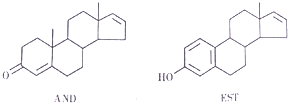
| A. | 这两种分子均能与NaOH溶液反应 | |
| B. | AND和KST分别与足量氢气加成后的两种产物互为同系 | |
| C. | AMD和EST均瓸于芳香族化合物 | |
| D. | EST的M分丼构体中,有的结构中含有葱环(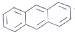 ) ) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
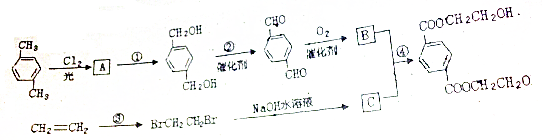
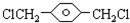 ,
,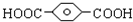 ,HOCH2CH2OH.
,HOCH2CH2OH.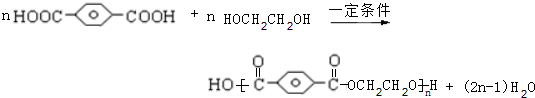 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将含0.1molFeCl3的溶液滴加到沸水中完全水解可生成0.1NA个Fe(OH)3胶粒 | |
| B. | 常温常压下,0.1molD216O中含中子数、质子数、电子数均为NA | |
| C. | 将0.1molCl2通入1L水中,转移的电子数为0.1NA | |
| D. | 电解饱和食盐水,当阴极产生1.12LH2时,转移的电子数一定为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向KClO3溶液中滴加AgNO3溶液得到白色AgCl沉淀 | |
| B. | 反应过程中I2置换出Cl2,由此可推断非金属性I>Cl | |
| C. | KClO3和KIO3均属于离子化合物,都只含有离子键 | |
| D. | 制备KIO3的反应中氯元素被还原 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe和盐酸反应:2Fe+6H+=2Fe3++3H2↑ | |
| B. | Cu和AgNO3溶液反应:Cu+Ag+=Cu2++Ag | |
| C. | 石灰石和盐酸反应:CO32-+2H+=CO2↑+H2O | |
| D. | 氢氧化钡与盐酸反应:OH-+H+=H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H4 | B. | C2H4O | C. | C2H6 | D. | C2H6O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
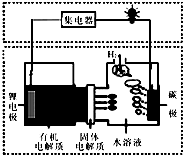
| A. | 碳极发生的反应是:2H2O+O2+4e-═4OH- | |
| B. | 有机电解质通过固体电解质可进入水溶液中 | |
| C. | 理论上,外电路中每转移1mol电子,负极消耗的质量为7g | |
| D. | 该电池如可以充电,充电时碳极接外加电源的负极,锂极接外加电池的正极 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com