
【题目】热化学:(1)已知:C(s)+H2O(l)=CO(g)+H2(g) ΔH1=a kJ·mol-1;
2CO(g)+O2(g)=2CO2(g) ΔH2=bkJ·moL-1;
2H2(g)+O2(g)=2H2O(l) ΔH3=ckJ·moL-1;
则C(s)+O2(g)=CO2(g) ΔH=___(用a、b、c表示)kJ·moL-1。
(2)根据键能数据估算CH4(g)+4F2(g)=CF4(g)+4HF(g)的反应热ΔH=___。
化学键 | C—H | C—F | H—F | F—F |
键能(kJ·mol-1) | 414 | 489 | 565 | 155 |
【答案】![]() (2a+b+c) -1940 kJ·mol-1
(2a+b+c) -1940 kJ·mol-1
【解析】
(1)根据盖斯定律分析计算;
(2)ΔH=反应物断裂化学键吸收的能量-生成物形成化学键放出的能量。
(1)C(s)+H2O(l)=CO(g)+H2(g) ΔH1=a kJ·mol-1 ①;
2CO(g)+O2(g)=2CO2(g) ΔH2=bkJ·moL-1 ②;
2H2(g)+O2(g)=2H2O(l) ΔH3=ckJ·moL-1 ③;
则根据盖斯定律可知,![]() (①
(①![]() 2+②+③)得到C(s)+O2(g)=CO2(g),因此ΔH=
2+②+③)得到C(s)+O2(g)=CO2(g),因此ΔH=![]() (2ΔH1+ΔH2+ΔH3)=
(2ΔH1+ΔH2+ΔH3)=![]() (2a+b+c) kJ·moL-1,故答案为:
(2a+b+c) kJ·moL-1,故答案为:![]() (2a+b+c);
(2a+b+c);
(2)结合表格数据,根据反应CH4(g)+4F2(g)=CF4(g)+4HF(g)可知,ΔH=4![]() 414 kJ·mol-1+4
414 kJ·mol-1+4![]() 155 kJ·mol-1-4
155 kJ·mol-1-4![]() 489 kJ·mol-1-4
489 kJ·mol-1-4![]() 565 kJ·mol-1=-1940 kJ·mol-1,故答案为:-1940 kJ·mol-1。
565 kJ·mol-1=-1940 kJ·mol-1,故答案为:-1940 kJ·mol-1。


 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案科目:高中化学 来源: 题型:
【题目】下列各有机物无论二者以什么比例混合,只要总物质的量一定,则完全燃烧生成H2O的质量和消耗氧气的质量不变的是( )
① 丙烷、丁炔 ② 丙烯、C4H6O2 ③ 乙炔、苯 ④ 甲醇、C3H4O5
A.①③B.①②C.②④D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备硝基苯,反应装置如图。下列对该实验的叙述错误的是
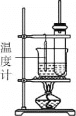
A.长玻璃管起冷凝回流作用
B.水浴加热其优点是受热均匀,便于控制温度
C.粗产品依次用蒸馏水和5%NaOH溶液洗涤,最后再用蒸馏水洗涤
D.洗涤后,用无水CaCl2干燥,然后过滤,得到纯硝基苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为甲烷晶体的晶胞结构,下列有关说法正确的是( )
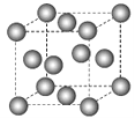
A.甲烷晶胞中的球体只代表一个碳原子
B.晶体中1个![]() 分子有12个紧邻的甲烷分子
分子有12个紧邻的甲烷分子
C.![]() 晶体熔化时需克服共价键
晶体熔化时需克服共价键
D.一个甲烷晶胞中含有8个![]() 分子
分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知电解NaOH溶液即电解水:2H2O![]() 2H2↑+O2↑。现对100g 11.7%的NaCl溶液进行电解,总共通过电子0.4mol。
2H2↑+O2↑。现对100g 11.7%的NaCl溶液进行电解,总共通过电子0.4mol。
(1)在阴极产生的氢气的体积(按标准状况计)为______
(2)阳极产生的氧气的物质的量为__________
(3)假定控制条件使Cl2未从电解液中逸出,电解结束后经充分搅拌Cl2与NaOH发生了完全反应,生成NaClO和部分NaClO3。求完全反应后电解池中三种钠盐的总质量____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E五种元素,它们的核电荷数依次增大。已知:A失去一个电子后就成为一个质子;B有两个电子层,其最外层的电子数是次外层电子数的2倍;C的L层得2个电子后成为稳定结构;D是海水中含量第一位的金属元素;E的最外层电子比次外层电子少一个。请填写下列空格:
(1)A形成的单质的结构式为______; BC2的电子式_______________。
(2)D离子的结构示意图_________,D、E结合形成的化合物的电子式_____
(3)B、C、D三种元素可形成一种化合物,其化学式为_____,所含的化学键有____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用0.1mol·L-1的NaOH溶液分别滴定相同浓度的弱酸HX、HY的稀溶液,其滴定曲线如图所示。下列说法错误的是( )
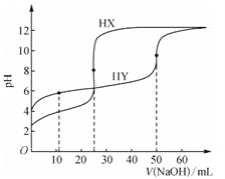
A.HX的酸性比HY的强B.滴定过程中,均可用酚酞作指示剂
C.室温下,Ka(HY)的数量级约为10-4 D.滴定前,HY的体积为HX的两倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝、钛、钡(第2主族)等元素在能源、材料等领域应用广泛。回答下列问题:
⑴与钛同周期的所有副族元素的基态原子中,最外层电子数与基态钛原子相同的元素有________种。基态Ti2+的最外层电子排布式为________________。
⑵铝的逐级电离能数据为:I1=580 kJmol-1、I2=1820 kJmol-1、I3=2750 kJmol-1、I4=11600 kJmol-1。请分析数据规律,预测钡的逐级电离能的第一个数据“突跃”点出现在________之间(用I1、I2、I3等填空![]() 。
。
⑶已知第ⅡA族元素的碳酸盐MCO3热分解的主要过程是:M2+结合碳酸根离子中的氧离子。则CaCO3、BaCO3的分解温度较高的是________________(填化学式),理由是________________。
⑷催化剂M能催化乙烯、丙烯、苯乙烯等的聚合,其结构如图1所示。
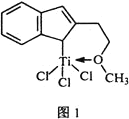
①M中,碳原子的杂化类型有________________。
②M中,不含________![]() 填标号
填标号![]() 。
。
A. π键 B. δ键 C. 配位键 D.氢键 E. 离子键
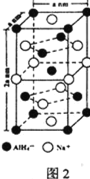
⑸氢化铝钠(NaAlH4)是一种新型轻质储氢材料,其晶胞结构如图2所示,为长方体。写出与AlH4-空间构型相同的一种分子_______________(填化学式)。NaAlH4晶体中,与AlH4-紧邻且等距的Na+有________个;NaAlH4晶体的密度为________ gcm-3(用含a、NA的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.火箭升空需要高能的燃料,经常是用N2O4和N2H4作为燃料,工业上利用N2和H2可以合成NH3,NH3又可以进一步制备联氨(N2H4)等。已知:
N2(g) + 2O2(g)=2NO2(g) △H= +67.7kJ·mol-1
N2H4(g) + O2(g)=N2(g) + 2H2O(g) △H=-534.0kJ·mol-1
NO2(g)![]() 1/2N2O4(g) △H=-26.35kJ·mol-1
1/2N2O4(g) △H=-26.35kJ·mol-1
试写出气态联氨在气态四氧化二氮中燃烧生成氮气和气态水的热化学方程式:___。
Ⅱ.1100℃时,体积为2L的恒容容器中发生如下反应:Na2SO4(s)+4H2(g)![]() Na2S(s)+4H2O(g)。
Na2S(s)+4H2O(g)。
(1)下列能判断反应达到平衡状态的是____。
A.容器中压强不变 B.混合气体密度不变
C.1molH-H键断裂同时形成2 mol H-O D.H2的体积分数不变
(2)若2min时反应达平衡,此时气体质量增加8g,则用H2表示该反应的反应速率为___。
(3)某温度下该反应达平衡状态,测得混合气体的平均相对分子质量为14,则该温度下的平衡常数K为_____。
(4)若反应达平衡后,加入少量的H2,再次平衡后,H2O的体积分数___(填“增大”、“减小”或“不变”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com