
【题目】一同学用某种粗盐进行提纯实验,步骤见下图.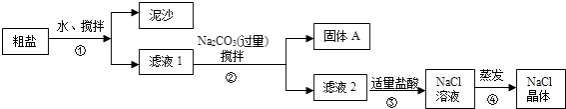
请回答:
(1)步骤①和②的操作名称是 .
(2)步骤③判断加入盐酸“适量”的方法是;步骤④加热蒸发时要用玻璃棒不断搅拌,这是为了防止 , 当蒸发皿中有较多量固体出现时,应 , 用余热使水分蒸干.
(3)猜想和验证:
猜想 | 验证的方法 | 现象 | 结论 |
猜想Ⅰ:固体A中含 | 取少量固体A于试管中,滴加稀盐酸,并用涂有澄清石灰水的小烧杯罩于试管口 |
| 猜想Ⅰ成立 |
猜想Ⅱ:固体A中含 | 取少量固体A于试管中,先滴入 , 再滴入Na2SO4溶液 | 有气泡放出,无白色沉淀 | |
猜想Ⅲ:最后制得的NaCl晶体中还含有Na2SO4 | 取少量NaCl晶体溶于试管中的蒸馏水, |
| 猜想Ⅲ成立 |
【答案】
(1)过滤
(2)滴加盐酸至无气泡放出为止;局部过热,造成固体(或溶液)飞溅;停止加热(或熄灭酒精灯)
(3)有气泡放出,烧杯底变浑浊(或石灰水变浑浊,或石灰水有白色沉淀);稀硝酸(或稀盐酸);猜想Ⅱ不成立;滴入BaCl2[或Ba(OH)2或Ba(NO3)2]溶液和稀HNO3;有白色沉淀且不溶于稀HNO3
【解析】解:(1)步骤①用于分离固体和液体,滤液Ⅰ中含有氯化钙,加入碳酸钠可生成碳酸钙沉淀,步骤②也是固体和液体的分离,则应用过滤的方法分离,所以答案是:过滤;(2)滤液②中含有过量的碳酸钠,加入盐酸时产生气泡,当滴加盐酸至刚好无气泡放出时说明恰好完好反应,盐酸量为适量;蒸发结晶时,注意:用玻璃棒不断搅拌,防止局部过热,造成固体(或溶液)飞溅;当蒸发皿中有较多量固体出现时,应停止加热,用余热使水分蒸干;
所以答案是:滴加盐酸至无气泡放出为止;局部过热,造成固体(或溶液)飞溅;停止加热(或熄灭酒精灯);(3)猜想Ⅰ:取少量固体A于试管中,滴加稀盐酸,并用涂有澄清石灰水的小烧杯罩于试管口,如有气泡放出,烧杯底变浑浊(或石灰水变浑浊),说明猜想Ⅰ成立;
猜想Ⅱ:稀硝酸(或稀盐酸);有气泡放出,无白色沉淀,说明猜想Ⅱ不成立;
猜想Ⅲ:滴入BaCl2[或Ba(OH)2或Ba(NO3)2]溶液和稀HNO3 , 有白色沉淀且不溶于稀HNO3 , 说明最后制得的NaCl晶体中还含有Na2SO4 , 则猜想Ⅲ成立,
所以答案是:
猜想 | 验证的方法 | 现象 | 结论 |
有气泡放出,烧杯底变浑浊(或石灰水变浑浊,或石灰水有白色沉淀) | |||
滴入稀硝酸(或稀盐酸) | 猜想Ⅱ不成立 | ||
滴入BaCl2[或Ba(OH)2或Ba(NO3)2]溶液和稀HNO3 | 有白色沉淀且不溶于稀HNO3 |


科目:高中化学 来源: 题型:
【题目】氯气是一种重要的工业原料,工业上利用反应3Cl2+2NH3=N2+6HCl检查氯气管道是否漏气,下列说法错误的是( )
A. 氧化产物为N2
B. 该反应NH3被还原
C. 该反应HCl是还原产物
D. 生成1 mol N2有6 mol电子转移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相同温度下,体积均为0.25L的两个恒容密闭容器中发生可逆反应:X2(g) + 3Y2(g) ![]() 2XY3(g) △H=-92.6kJ/mol
2XY3(g) △H=-92.6kJ/mol
实验测得反应在起始、达到平衡时的有关数据如下表所示:
容器 编号 | 起始时各物质物质的量/mol | 达平衡时体系能量的变化 | ||
X2 | Y2 | XY3 | ||
① | 1 | 3 | 0 | 23.15 kJ |
② | 0.6 | 1.8 | 0.8 | Q kJ |
下列叙述正确的是
A. 容器①、②中反应的平衡常数不相等
B. 达平衡时,两个容器中XY3的物质的量浓度均为2 mol/L
C. 容器②中反应达到平衡时放出的热量为23.15kJ
D. 若容器①体积为0.20 L,则达平衡时放出的热量小于23.15 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关细胞内元素和化合物之最的说法,正确的是
A. 鲜重的最基本元素是O元素,干重的最基本元素是C元素
B. 小麦细胞中含量最多的干物质是淀粉
C. 骨骼肌细胞中含量最多的化合物是蛋白质
D. 肥胖患者的细胞中含量最多的化合物是脂肪
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图虚线框中的装置可用来检验浓硫酸与木炭粉在加热条件下反应产生的所有气体产物,填写下列空白:
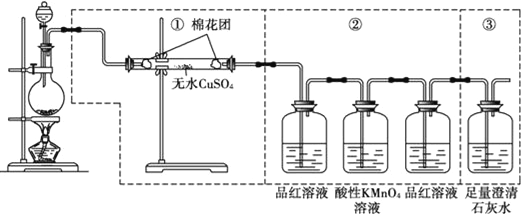
(1)装置中①、②、③可以检验出的物质是①__,②__,③__.
(2)浓硫酸与木炭粉反应的化学方程式:__.
(3)②中第一瓶品红溶液的作用是__,第二瓶品红溶液的作用是__,酸性KMnO4溶液的作用是_____________.
(4)证明产生的气体中含有CO2的现象是:___________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色工业废水中可能含有Na+、Mg2+、Al3+、Cu2+、Cl﹣、SO42﹣中的几种离子.
a.取0.1mL该废水于管中,加入足量的Ba(N03)溶液和稀硝酸,产生白色沉淀,充分反应后过滤,向滤液中加入AgNO3溶液无沉淀产生.
b.另取10mL该废水于管中,滴加NaOH溶液先产生白色沉淀,后部分沉淀溶解.生成沉淀的物质的量随加入NaOH物质的量关系如图所示.

根据上述实验和图表数据:
(1)该废水中一定不含有的离子有______________(填离子符号).
(2)实验室配制100mL1molL﹣1的NaOH溶液时,用到的玻璃仪器除烧杯、玻璃棒、量筒外,还需要_____________(填仪器名称).
(3)写出A→B过程中发生反应的离子方程式:_________________________.
(4)该废水中,c(Al3+)=_______________________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com