
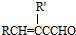 +H2O(R、R′表示烃基或氢),高分子化合物PVB的合成就是其一种重要应用.
+H2O(R、R′表示烃基或氢),高分子化合物PVB的合成就是其一种重要应用.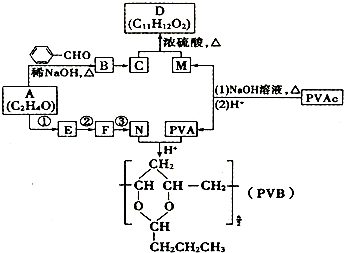

 合成B的化学方程式是
合成B的化学方程式是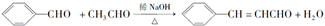 .
.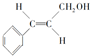 .
.分析 A的分子式为C2H4O,与苯甲醛反应得到B,结合信息可知,A为CH3CHO,B为 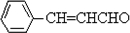 ,C为反式结构,由B还原得到,可以确定C中仍具有C=C,被还原的基团应是-CHO,可确定C的结构式
,C为反式结构,由B还原得到,可以确定C中仍具有C=C,被还原的基团应是-CHO,可确定C的结构式 ,根据D的分子式C11H12O2,可以确定其不饱和度为6,结合生成D的反应条件,可确定D为
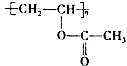
,根据D的分子式C11H12O2,可以确定其不饱和度为6,结合生成D的反应条件,可确定D为  ,进而确定M为CH3COOH.由PVB的结构简式和题给信息I可确定其单体之一是CH3(CH2)2CHO,即N为CH3(CH2)2CHO,另一高分子化合物PVA为
,进而确定M为CH3COOH.由PVB的结构简式和题给信息I可确定其单体之一是CH3(CH2)2CHO,即N为CH3(CH2)2CHO,另一高分子化合物PVA为 ,进而推出PVAc的单体为CH3COOCH=CH2;由A和N的结构简式,结合题给信息,可推出E为CH3CH=CHCHO,F为CH3(CH2)3OH,据此解答.
,进而推出PVAc的单体为CH3COOCH=CH2;由A和N的结构简式,结合题给信息,可推出E为CH3CH=CHCHO,F为CH3(CH2)3OH,据此解答.
解答 解:A的分子式为C2H4O,与苯甲醛反应得到B,结合信息可知,A为CH3CHO,B为 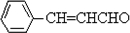 ,C为反式结构,由B还原得到,可以确定C中仍具有C=C,被还原的基团应是-CHO,可确定C的结构式
,C为反式结构,由B还原得到,可以确定C中仍具有C=C,被还原的基团应是-CHO,可确定C的结构式 ,根据D的分子式C11H12O2,可以确定其不饱和度为6,结合生成D的反应条件,可确定D为
,根据D的分子式C11H12O2,可以确定其不饱和度为6,结合生成D的反应条件,可确定D为  ,进而确定M为CH3COOH.由PVB的结构简式和题给信息I可确定其单体之一是CH3(CH2)2CHO,即N为CH3(CH2)2CHO,另一高分子化合物PVA为
,进而确定M为CH3COOH.由PVB的结构简式和题给信息I可确定其单体之一是CH3(CH2)2CHO,即N为CH3(CH2)2CHO,另一高分子化合物PVA为 ,进而推出PVAc的单体为CH3COOCH=CH2;由A和N的结构简式,结合题给信息,可推出E为CH3CH=CHCHO,F为CH3(CH2)3OH.
,进而推出PVAc的单体为CH3COOCH=CH2;由A和N的结构简式,结合题给信息,可推出E为CH3CH=CHCHO,F为CH3(CH2)3OH.
(1)PVAc由一种单体经加聚反应得到,该单体的结构简式是:CH3COOCH=CH2,
故答案为:CH3COOCH=CH2;
(2)A为CH3CHO,核磁共振氢谱有2组吸收峰,
故答案为:2;
(3)E为CH3CH=CHCHO,E的名称为:2-丁烯醛,
故答案为:2-丁烯醛;
(4)A与 合成B的化学方程式是:
合成B的化学方程式是: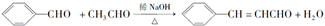 ,
,
故答案为: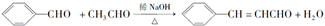 ;
;
(5)由上述分析可知,则C的反式结构是: ,
,
故答案为: ;
;
(6)根据PVB的结构简式,结合信息可推出N的结构简式是CH3(CH2)2CHO,又因为E能使Br2的CCl4溶液褪色,所以E是2分子乙醛在氢氧化钠溶液中并加热的条件下生成的,即E的结构简式是CH3CH=CHCHO,然后E通过氢气加成得到F,所以F的结构简式是CH3CH2CH2CH2OH.F经过催化氧化得到N,反应方程式为:2CH3(CH2)3OH+O2$→_{△}^{Cu}$2CH3(CH2)2CHO+2H2O,
故答案为:稀NaOH、加热;加成反应;2CH3(CH2)3OH+O2$→_{△}^{Cu}$2CH3(CH2)2CHO+2H2O.
点评 本题考查有机物的推断与合成,充分利用给予的信息、有机物结构与分子式进行推断,需要学生熟练掌握官能团的性质与转化,较好的考查学生自学能力、知识迁移运用能力,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 不慎将浓碱溶液沾到皮肤上,立即用大量硫酸冲洗,然后再用水冲洗 | |
| B. | 不慎将酸溅到眼中,立即用大量水冲洗,边洗边眨眼睛 | |
| C. | 实验时手指上不小心沾上浓硫酸,立即用NaOH溶液清洗 | |
| D. | 酒精不慎洒在实验桌上烧起来时,立即用水浇灭 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
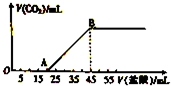 将5.08g由Na2CO3和NaHCO3组成的固体混合物完全溶于水,制成溶液,然后向该溶液中逐滴加入2mol?L-1的盐酸,所加入盐酸的体积与产生CO2体积(标准状况)的关系如图所示.
将5.08g由Na2CO3和NaHCO3组成的固体混合物完全溶于水,制成溶液,然后向该溶液中逐滴加入2mol?L-1的盐酸,所加入盐酸的体积与产生CO2体积(标准状况)的关系如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某同学组装了如图所示的电化学装置.电极Ⅰ为Al,其他电极均为Cu.
某同学组装了如图所示的电化学装置.电极Ⅰ为Al,其他电极均为Cu.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
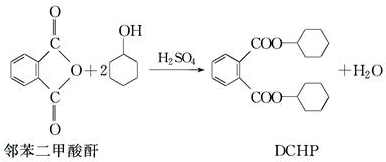
| A. | 邻苯二甲酸酐属于酸性氧化物 | |
| B. | 环己醇分子中所有的原子可能共平面 | |
| C. | DCHP能发生加成、取代、消去反应 | |
| D. | 1molDCHP最多可与含2molNaOH的烧碱溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
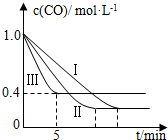 利用甲烷与水反应制备氢气,因原料廉价产氢率高,具有实用推广价值.
利用甲烷与水反应制备氢气,因原料廉价产氢率高,具有实用推广价值.| 编号 | 温度 | 压强 | c始(CO) | c始(H2O) |
| Ⅰ | 530℃ | 3MPa | 1.0mol•L-1 | 3.0mol•L-1 |
| Ⅱ | X | Y | 1.0mol•L-1 | 3.0mol•L-1 |
| Ⅲ | 630℃ | 5MPa | 1.0mol•L-1 | 3.0mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 的链节为
的链节为 .其单体的结构简式分别为
.其单体的结构简式分别为 、
、 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
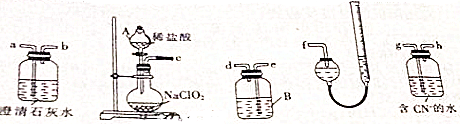

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com