
现有反应aA(g)+bB(g)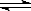 pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
(1)该反应的逆反应是_______热反应,且a+b______p(填“>”“<”或“=”)。
(2)减压时,A的质量分数________(填“增大”“减小”或“不变”,下同),正反应速率________。
(3)若加入B(体积不变),则A的转化率________,B的转化率________。
(4)若升高温度,则平衡时,B、C的浓度之比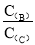 将________。
将________。
(5)若加入催化剂,平衡时气体混合物的总物质的量________。
(6)若B是有色物质,A、C均为无色物质,则加入C(体积不变)时混合物的颜色________,而维持容器体积不变,充入氖气时,混合物的颜色________(填“变浅”“变深”或“不变”)。
(1)放;>;(2)增大;减小;(3)增大;减小;(4)减小;(5)不变;(6)变深;不变
【解析】
试题分析:(1)根据勒夏特列原理,升高温度,B的转化率变大,说明平衡向正反应方向进行,正反应为吸热反应,则逆反应方向是放热反应;减小压强,C的质量分数减小,说明平衡向逆反应方向进行,即a+b>p。(2)减压,平衡向气体体积增加的方向进行,据(1)得知a+b>p,因此平衡逆向进行,A的质量分数增大;减压,反应速率减小。(3)加入B,增加了反应物浓度,化学平衡右移,A的转化率增大,虽然平衡右移,但对B物质来说,消耗的多了,总物质的量也增加了,因此转化率减小。(4)根据(1)得知,正反应方向是吸热反应,升高温平衡右向移动,c(C)增大、c(B)减小,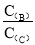 减小。(5)催化剂只改变反应速率,对化学平衡的移动无影响,平衡时气体混合物的总物质的量不变;(6)加入C,B的浓度增大,颜色加深;等容充入氖气,随压强增加,但各组分的浓度不变,平衡不移动,颜色不变。
减小。(5)催化剂只改变反应速率,对化学平衡的移动无影响,平衡时气体混合物的总物质的量不变;(6)加入C,B的浓度增大,颜色加深;等容充入氖气,随压强增加,但各组分的浓度不变,平衡不移动,颜色不变。
考点:考查影响化学平衡的因素等相关知识。


科目:高中化学 来源:2014-2015福建省等四校高一上学期期中联考化学试卷(解析版) 题型:选择题
下列溶液中氯离子的物质的量浓度与50 mL 1 mol/L的AlCl3溶液中氯离子的物质的量浓度相等的是
A.75 mL 2 mol/L的CaCl2 B.150 mL 3 mol/L的KCl
C.150 mL 1 mol/L的NaCl D.75mL 2 mol/L的NH4Cl
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海理工大学附中高三上学期月考化学试卷(解析版) 题型:选择题
下列有关化学用语使用正确的是
A.次氯酸的结构式: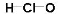
B.CO2的比例模型 
C.甲基的电子式: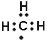
D.硬脂酸的化学式:C17H33COOH
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省等七校高三12月联考理综化学试卷(解析版) 题型:填空题
过氧化钙可以用于改善地表水质,处理含重金属粒子废水和治理赤潮,也可用于应急供氧等。工业上生产过氧化钙的主要流程如下:
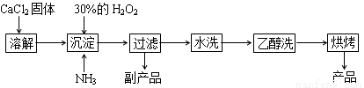
已知:CaO2·8H2O是一种白色固体,微溶于水,加热至350 ℃左右开始分解放出氧气。
(1)完成用上述方法制取CaO2·8H2O的化学方程式是:CaCl2+H2O2+2NH3+8H2O==CaO2·8H2O↓+________;
(2)检验“水洗”是否合格的操作方法是_________________________________________;
(3)沉淀时常用冰水控制温度在0 ℃左右,其可能原因是(写出两种):
① ; ②____________________________。
(4)测定产品中CaO2的含量的实验步骤:【已知:I2+2S2O32-=2I-+S4O62-】
第一步:准确称取a g产品于有塞锥形瓶中,加入适量蒸馏水和过量的b g KI晶体,再滴入少量2 mol·L-1的H2SO4溶液,充分反应。
第二步:向上述锥形瓶中加入几滴淀粉溶液。
第三步:逐滴加入浓度为c mol·L-1的Na2S2O3溶液至反应完全,消耗Na2S2O3溶液V mL。
①CaO2的质量分数为____________(用字母表示);
②某同学第一步和第二步的操作都很规范,第三步滴速太慢,这样测得的CaO2的质量分数可能________(填“不受影响”、“偏低”或“偏高”),原因是___________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省等七校高三12月联考理综化学试卷(解析版) 题型:选择题
设nA为阿伏加德罗常数的数值。下列说法正确的是
A.2mol·L-1的AlCl3溶液中含Cl-数为6nA
B.常温常压下,14g氮气含有的核外电子数为7nA
C.铝跟氢氧化钠溶液反应生成1mol氢气时,转移的电子数为nA
D.高温高压下,28gN2与6gH2反应,生成的NH3分子数为2nA
查看答案和解析>>
科目:高中化学 来源:2014-2015学年内蒙古巴市高二10月月考化学试卷(解析版) 题型:选择题
某温度下,反应SO2(g)+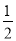 O2(g)
O2(g) SO3(g)的平衡常数K1=50,在同一温度下,反应2SO3(g)
SO3(g)的平衡常数K1=50,在同一温度下,反应2SO3(g) 2SO2(g)+O2(g)的平衡常数K2的值为
2SO2(g)+O2(g)的平衡常数K2的值为
A.2500 B.100 C.4×10-4 D.2×10-2
查看答案和解析>>
科目:高中化学 来源:2014-2015学年内蒙古巴市高二10月月考化学试卷(解析版) 题型:选择题
下列反应中生成物总能量高于反应物总能量的是
A.碳酸钙受热分解 B.乙醇燃烧
C.铝粉与氧化铁粉末反应 D.氧化钙溶于水
查看答案和解析>>
科目:高中化学 来源:2014-2015学年内蒙古巴市高二10月月考化学试卷(解析版) 题型:选择题
已知热化学方程式:SO2(g)+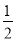 O2(g)
O2(g)  SO3(g) △H = ―98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为
SO3(g) △H = ―98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为
A.196.64kJ B.196.64kJ/mol
C.<196.64kJ D.>196.64kJ
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com