
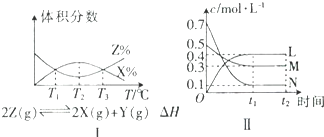
| A、由图Ⅰ可知,该反应在T2时达到平衡 |
| B、由Ⅰ图可知,该反应的△H<0 |
| C、图Ⅱ发生反应的化学方程式为2M+6N?3L |
| D、由图Ⅱ可知,若密闭容器中M、N、L的起始浓度依次为0.4mol/L、0.4mol/L、0.2mol/L,保持其他条件不变,达到平衡时L的浓度为0.4mol/L |
| c2(L) |
| c(M)c3(N) |
| 0.42 |
| 0.13×0.3 |
| (0.2+2x)2 |
| (0.4-x)×(0.4-3x)3 |
| 0.42 |
| 0.13×0.3 |


 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
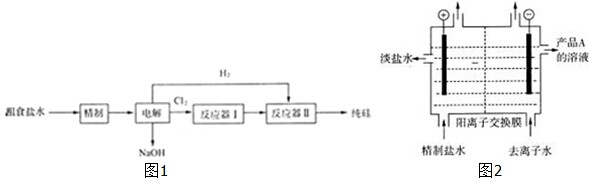
科目:高中化学 来源: 题型:
| A、2.24L |
| B、3.36L |
| C、4.48L |
| D、5.60L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、滴定时,使用酚酞作指示剂,溶液颜色恰好由无色变为浅红色,且半分钟内不褪色时,为滴定终点 |
| B、滴定时眼睛要注视着滴定管内NaOH溶液的液面变化,防止滴定过量 |
| C、碱式滴定管若滴定前平视读数、滴定后俯视读数,则测定结果偏高 |
| D、锥形瓶用水洗净后未用食醋润洗,则测得的食醋浓度偏低 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 试管内试剂 | 管口湿润的试纸 | 实验现象 | 实验结论 |
| A | 碘水 | 淀粉试纸 | 变蓝 | 碘具有氧化性 |
| B | 浓氨水,生石灰 | 蓝色石蕊试纸 | 变红 | 氨气为碱性气体 |
| C | Na2SO3,硫酸 | 品红试纸 | 褪色 | SO2具有漂白性 |
| D | Cu,稀硝酸 | KI-淀粉试纸 | 变蓝 | NO具有氧化性 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、水晶瓶可存放氢氟酸 |
| B、水玻璃存放在胶塞细口无色玻璃瓶中 |
| C、绿矾溶液可长期存放,不必现用现配 |
| D、氯水存放在胶塞细口棕色玻璃瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com