
| A、2.8 g乙烯和丙烯的混合物中所含碳原子数为0.2NA |
| B、4.48 L H2和O2的混合物中所含分子数为0.2NA |
| C、4 g重水(D2O)中所含质子数为0.2NA |
| D、200 mL 1 mol/L的氨水中含NH3?H2O分子数为0.2NA |
| m |
| M |
| 2.8g |
| 14g/mol |
| 4g |
| 20g/mol |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、锌锰干电池工作一段时间后碳棒不变 |
| B、燃料电池可将热能直接转变为电能 |
| C、燃料电池工作时燃料在负极被还原 |
| D、太阳能电池的主要材料是高纯度的二氧化硅 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、自来水 |
| B、0.5mol/L盐酸 |
| C、0.5mol/LCH3COOH |
| D、0.5mol/LNH4Cl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、-441.8kJ/mol |
| B、-520.8kJ/mol |
| C、-883.6kJ/mol |
| D、-260.4kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、氯原子的结构示意图: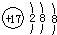 | ||
B、作为相对原子质量测定标准的碳核素:
| ||
C、氯化镁的电子式: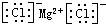 | ||
| D、乙烯的结构简式:CH2CH2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2.3gNa在足量的O2中完全燃烧和与在空气中缓慢反应完全,转移的电子数均为0.1NA |
| B、11.2LCl2所含的原子数为NA |
| C、化学上定义12g碳中的碳原子数为NA的数值 |
| D、1L 0.10mol/L的CuSO4溶液中含Cu2+数目为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
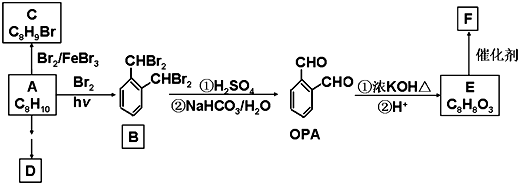

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com