
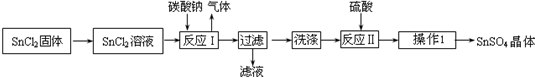
���� SnCl2�ܽ�õ���Һ����̼���Ƴ��������ӣ����˵õ�����ϴ�Ӻ���������ܽ�õ���������Һ������Ũ����ȴ�ᾧ������ϴ�ӵõ����������壮
��1����ԭ�ӵĺ˵����Ϊ50����̼Ԫ������ͬһ���壬���ڢ�A�壬����ԭ��������ȥ����������Ԫ������ȷ�����ڵ����ڣ�
��2������Ϣ��֪��SnCl2��ˮ�����ɼ�ʽ�Ȼ��������������ᣬ����Sn2+ˮ�⣬Sn2+�ױ�����������Sn�۳�������ҺpH�⣬����ֹSn2+��������
��3����Ӧ��õ�������SnO��SnԪ�ػ��ϼ�Ϊ�仯�����ڷ�������ԭ��Ӧ��ͬʱ�������壬������Ϊ������̼��
��4��ϴ�ӳ����ڹ���װ���н��У�
��5��������Һ��þ���ķ���������Ũ������ȴ�ᾧ�����ˡ�ϴ�����ش�
��6�����������£�SnSO4����������˫��ˮȥ������˫��ˮ��ǿ�����ԣ���Sn2+�ױ�����ΪSn4+����������ԭΪˮ��
��7�����ݵ���ת���غ��뷽��ʽ�ɵù�ϵʽSn2+��2Fe3+��2Fe2+��$\frac{1}{3}$K2Cr2O7���ݴ˼��㣮
��� �⣺��1����Ԫ����̼Ԫ������ͬһ���壬���ڢ�A�壬ԭ�Ӻ˵����Ϊ50����50-2-8-8-18=14����Sn���ڵ������ڣ��������ڱ��е�λ��Ϊ�������ڵڢ�A�壬
�ʴ�Ϊ���������ڵڢ�A�壮
��2������Ϣ��֪��SnCl2ˮ�⣬����SnCl2+H2O?Sn��OH��Cl+HCl���������ᣬʹ��ƽ�������ƶ�������Sn2+ˮ�⣬Sn2+�ױ�����������Sn�۳�������ҺpH�⣬����ֹSn2+����������SnCl2��������SnCl2��Һ�ķ����ǣ���SnCl2��������Ũ���ᣬ��ˮϡ��������Ũ�ȣ��ټ�������Sn�ۣ�
�ʴ�Ϊ����SnCl2��������Ũ���ᣬ��ˮϡ��������Ũ�ȣ��ټ�������Sn�ۣ�
��3����Ӧ��õ�������SnO��SnԪ�ػ��ϼ�Ϊ�仯�����ڷ�������ԭ��Ӧ��ͬʱ�������壬������Ϊ������̼�����ӷ���ʽΪ��Sn2++CO32-�TSnO��+CO2����
�ʴ�Ϊ��Sn2++CO32-�TSnO��+CO2����
��4��ϴ��SnO�����ķ��������ù���װ�ý���ϴ�ӣ���������м�������ˮ����û��������ˮ��ȫ�������ظ�����2-3�Σ�
�ʴ�Ϊ����������м�������ˮ����û��������ˮ��ȫ�������ظ�����2-3�Σ�
��5������������Һ��þ��壬��ȡ�ķ����ǣ�����Ũ������ȴ�ᾧ�����ˡ�ϴ�ӣ��ʴ�Ϊ������Ũ������ȴ�ᾧ�����ˡ�ϴ�ӣ�
��6�����������£�SnSO4����������˫��ˮȥ������˫��ˮ��ǿ�����ԣ���Sn2+�ױ�����ΪSn4+����������ԭΪˮ�����ӷ���ʽΪ��Sn2++H2O2+2H+�TSn4++2H2O��
�ʴ�Ϊ��Sn2++H2O2+2H+�TSn4++2H2O��
��7����ʵ����̿�֪�������ķ�ӦΪ��2Fe3++Sn2+=Sn4++2Fe2+��6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O����
Sn2+��2Fe3+��2Fe2+��$\frac{1}{3}$K2Cr2O7
1 $\frac{1}{3}$
n 0.0250L��0.100mol/L
���n=0.0075mol��
100ml��Һ�к���SnCl2 ���ʵ���=0.0075mol��$\frac{100}{25}$=0.03mol��
SnCl2����Ĵ���=$\frac{190g/mol��0.03mol}{6.1g}$��100%=93.44%��
��SnCl2����Ĵ���Ϊ93.44%��
���� ���⿼�������ʷ���ķ�����ʵ�������ˮ�����Ӧ�ã��ζ�ʵ��ļ����жϺͼ���Ӧ�ã����ջ����ǹؼ�����Ŀ�Ѷ��еȣ�


 ȫ�ܲ��һ���þ�ϵ�д�
ȫ�ܲ��һ���þ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
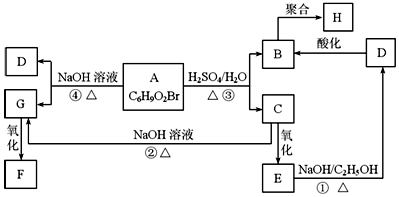 �л���A��B��C��D��E��F��G��H�ת����ϵ��ͼ��ʾ��5.2g F����100mL 1mol/L NaOH��Һǡ����ȫ�кͣ�0.1molF����������NaHCO3��Ӧ�ڱ�״���·ų�4.48LCO2��D�ķ���ʽΪC3H3O2Na��E�ķ����к����Ȼ���
�л���A��B��C��D��E��F��G��H�ת����ϵ��ͼ��ʾ��5.2g F����100mL 1mol/L NaOH��Һǡ����ȫ�кͣ�0.1molF����������NaHCO3��Ӧ�ڱ�״���·ų�4.48LCO2��D�ķ���ʽΪC3H3O2Na��E�ķ����к����Ȼ���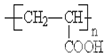 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
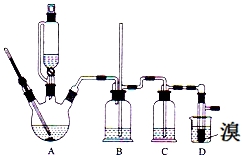 ʵ����������������������Ҵ���Ũ�����Ʊ�1��2-���������װ����ͼ��ʾ�����п��ܴ��ڵ���Ҫ����Ӧ�У��Ҵ���Ũ����Ĵ�������140����ˮ�������ѣ��й������б����£�
ʵ����������������������Ҵ���Ũ�����Ʊ�1��2-���������װ����ͼ��ʾ�����п��ܴ��ڵ���Ҫ����Ӧ�У��Ҵ���Ũ����Ĵ�������140����ˮ�������ѣ��й������б����£�| �Ҵ� | 1��2-�������� | ���� | |
| ״̬ | ��ɫҺ�� | ��ɫҺ�� | ��ɫҺ�� |
| �ܶ�/g•cm-3 | 0.79 | 2.2 | 0.71 |
| �е�/�� | 78.5 | 132 | 34.6 |
| �۵�/�� | -l30 | 9 | -1l6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
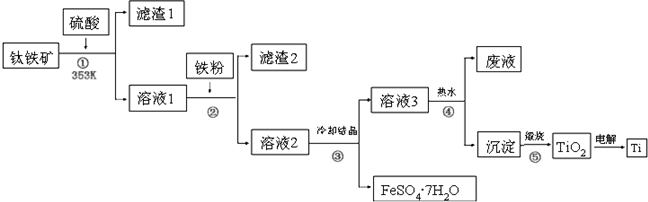
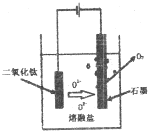
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
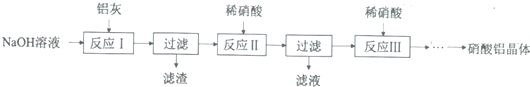
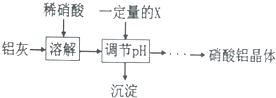
| �������� | Fe��OH��3 | Al��OH��3 |
| ��ʼ����pH | 1.9 | 4.2 |
| ������ȫpH | 3.2 | 5.4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
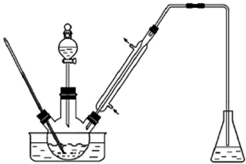 ʵ�����Ա���ȩΪԭ���Ʊ����屽��ȩ��ʵ��װ����Ҫ������ͼ��������ʵķе��������������������ʵķе㣨101kPa��
ʵ�����Ա���ȩΪԭ���Ʊ����屽��ȩ��ʵ��װ����Ҫ������ͼ��������ʵķе��������������������ʵķе㣨101kPa��| ���� | �е�/�� | ���� | �е�/�� |
| �� | 58.8 | 1��2-�������� | 83.5 |
| ����ȩ | 179 | ���屽��ȩ | 229 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
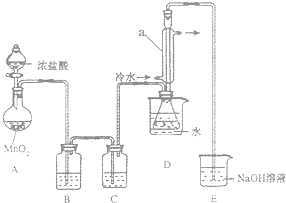 S2Cl2��һ�ֽ��ɫ�ӷ���Һ�壬������������ij��ѧ��ȤС�� �����ʵ���Ʊ�������S2Cl2����������֪S2Cl2��ˮ�������绯��Ӧ��һ������Ԫ�ػ� �ϼ����ߣ���һ���ֻ��ϼ۽��ͣ����������������ʺ��������Cl2��Ӧ��������S2Cl2����Ӧ�Ļ�ѧ����ʽΪ��2S+Cl2$\frac{\underline{\;\;��\;\;}}{\;}$S2Cl2��
S2Cl2��һ�ֽ��ɫ�ӷ���Һ�壬������������ij��ѧ��ȤС�� �����ʵ���Ʊ�������S2Cl2����������֪S2Cl2��ˮ�������绯��Ӧ��һ������Ԫ�ػ� �ϼ����ߣ���һ���ֻ��ϼ۽��ͣ����������������ʺ��������Cl2��Ӧ��������S2Cl2����Ӧ�Ļ�ѧ����ʽΪ��2S+Cl2$\frac{\underline{\;\;��\;\;}}{\;}$S2Cl2��| ���� | S | S2Cl2 |
| �е�/�� | 445 | 138 |
| �۵�/�� | 113 | -76 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
| �� ���� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | 0 |
| 2 | �� | �� | ||||||
| 3 | �� | �� | �� | �� | �� | �� |
 ��
�� ��
�� ���γɵľ��������Ӿ��壮
���γɵľ��������Ӿ��壮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 10min�ڣ���Ӧ�ų�������Ϊ197kJ���� | |
| B�� | 10min�ڣ�X��ƽ����Ӧ����Ϊ0.06mol•L-1•min-1 | |
| C�� | ��10minʱ��Y�ķ�Ӧ����С��0.015mol•L-1•min-1��������ϵ�¶Ȳ��䣩 | |
| D�� | ��10minʱ��ZŨ��Ϊ0.6mol•L-1 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com