
【题目】目前世界上60%的镁是从海水中提取的。海水提镁的主要流程如下:
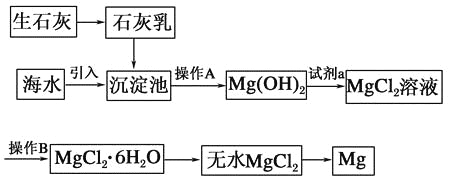
请回答下列问题:
(1)从离子反应的角度思考,在海水中加入石灰乳的作用是________,写出在沉淀池中发生反应的离子方程式:_________________________________________________。
(2)石灰乳是生石灰与水形成的化合物,从充分利用海洋化学资源,提高经济效益的角度考虑,生产生石灰的主要原料来源于海洋中的________。
(3)操作A是________,操作B是________。
(4)加入的足量试剂a是________(填化学式)。
(5)无水MgCl2在熔融状态下,通电后会产生Mg和Cl2,该反应的化学方程式为________,从考虑成本和废物循环利用的角度,副产物氯气可以用于________。
【答案】(1)沉淀Mg2+[或使Mg2+形成Mg(OH)2沉淀] Mg2++2OH-===Mg(OH)2↓
(2)贝壳(或牡蛎壳等) (3)过滤 加热浓缩(或蒸发结晶)
(4)HCl (5)MgCl2(熔融)![]() Mg+Cl2↑ 制盐酸,循环使用
Mg+Cl2↑ 制盐酸,循环使用
【解析】
(1)石灰乳中的Ca(OH)2与海水中的镁盐发生复分解反应生成Mg(OH)2沉淀。
(2)海滩上贝壳的主要成分是CaCO3,可用于制取生石灰。
(3)从沉淀池中得到Mg(OH)2固体,应利用过滤操作,加热浓缩MgCl2溶液,可使其结晶出MgCl2晶体。
(4)溶解Mg(OH)2应用足量盐酸。
(5)MgCl2(熔融)![]() Mg+Cl2↑,Cl2可用于生产盐酸,循环利用。
Mg+Cl2↑,Cl2可用于生产盐酸,循环利用。


科目:高中化学 来源: 题型:
【题目】下列有关说法不正确的是( )
A.太阳能以光和热的形式传送到地面,人们可以直接利用这些光和热
B.反应热就是化学反应中放出的能量
C.煤中含有硫元素,大量直接燃烧煤会引起酸雨等环境问题
D.等量的硫蒸气和硫固体分别完全燃烧,前者放出的热量多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家研发了一种室温下“可呼吸”的Na—CO2二次电池。将NaClO4溶于有机溶剂作为电解液,钠和负载碳纳米管的镍网分别作为电极材料,电池的总反应为:3CO2+4Na![]() 2Na2CO3+C。下列说法错误的是
2Na2CO3+C。下列说法错误的是

A. 放电时,ClO4-向负极移动
B. 充电时释放CO2,放电时吸收CO2
C. 放电时,正极反应为:3CO2+4e =2CO32-+C
D. 充电时,正极反应为:Na++e=Na
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学-选修5:有机化学基础]有机化合物F是一种重要的有机合成中间体,其合成路线如下图所示:

已知:①A的核磁共振氢谱图中显示两组峰②F的结构简式为:

③通常在同一个碳原子上连有两个羟基不稳定,易脱水形成羰基。
④![]()
请回答下列问题:
(1)A的名称为______________(系统命名法);Z中所含官能团的名称是___________。
(2)反应Ⅰ的反应条件是__________;反应Ⅲ的反应类型为__________ 。
(3)E的结构简式为_______________________。
(4)写出反应Ⅴ的化学方程式____________________________________________。
(5)写出反应IV中的化学方程式____________________________________________。
(6)W是Z的同系物,相对分子质量比Z大14,则W的同分异构体中满足下列条件:
①能发生银镜反应,②苯环上有两个取代基,③不能水解,遇FeCl3溶液不显色的结构共有_________种(不包括立体异构),核磁共振氢谱有四组峰的结构为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图装置中,容器甲内充入0.1 mol NO气体。干燥管内装有一定量Na2O2,从A处缓慢通入CO2气体。恒温下,容器甲中活塞缓慢由D处向左移动,当移至C处时容器体积缩至最小,为原体积9/10,干燥管中物质的质量增加了2.24 g。随着CO2的继续通入,活塞又逐渐向右移动。下列说法中正确的是

A. 活塞从D处移动到C处的过程中,通入的CO2气体为2.24 L(标准状况)
B. NO2转化为N2O4的转化率为20%
C. 容器甲中NO已反应完
D. 活塞移至C处后,继续通入a mol CO2,此时活塞恰好回至D处,则a小于0.01
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2S2O3是一种弱酸,实验室欲用0.01 mol/L的Na2S2O3溶液滴定碘水,发生的反应为I2+2Na2S2O3===2NaI+Na2S4O6,下列说法正确的是( )
A. 该滴定反应可用甲基橙作指示剂
B. Na2S2O3是该反应的还原剂
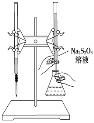
C. 该滴定反应可选用如下图所示的装置
D. 该反应中每消耗2 mol Na2S2O3,转移电子的物质的量为4 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若NA表示阿伏加德罗常数的值,下列叙述中正确的是
A. 常温下,9.2gNO2和N2O4的混合气体中含有的氮原子数目为0.2NA
B. 22.4L N2与CO组成的混合气体所含有的电子数为14NA
C. 0.1mol/L K2CO3溶液中所含K+数目为0.2NA
D. 在反应KClO3+6HCl=KCl+3Cl2↑+3H2O中,每生成3molCl2转移的电子数为6NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请根据表格中提供的甲、乙、丙、丁四种元素的相关信息完成下列问题:
元素 | 甲 | 乙 | 丙 | 丁 |
原子序数 | 11 | ③ | ||
元素符号 | ② | S | ||
原子结构示意图 | ① |
| ||
元素周期表中的位置 | 第三周期第ⅢA族 | ④ |
(1)填写表格中各序号所对应的空白:①_________________②__________________
③_________________④_________________。
(2)甲、乙、丙、丁四种元素中,原子半径最大的是____________(填元素符号),丁元素的最高正价为______________价。
(3)元素的最高价氧化物对应水化物中碱性最强的是_________(填化学式,下同), 呈两性的氢氧化物是__________________,酸性最强的是__________________。
(4)最高价氧化物对应水化物的碱性:甲_______________乙(填“>”或“<”),简单气态氢化物的稳定性:丙_______________丁(填“>”或“<”)。
(5)元素乙的最高价氧化物对应水化物,既能与元素甲的最高价氧化物对应水化物反应,又能中和过多的胃酸。请写出中和胃酸的离子方程式:_________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com