
| A. | 11.6g | B. | 10.8g | C. | 8.4g | D. | 13.2g |
分析 加入1mol•L-1硫酸溶液200mL时,固体恰好完全溶解,所得溶液中不含Fe3+,溶质为硫酸铜、硫酸亚铁,反应生成水,由n(H2SO4)=n(H2O)=n(混合物中O),结合用足量的CO在高温下还原相同质量的原混合物,得到固体质量为14.8g-m(O)计算.
解答 解:加入1mol•L-1硫酸溶液200mL时,固体恰好完全溶解,所得溶液中不含Fe3+,溶质为硫酸铜、硫酸亚铁,反应生成水,
由n(H2SO4)=n(H2O)=n(混合物中O),可知混合物中含n(O)=0.2L×1mol/L=0.2mol,
结合用足量的CO在高温下还原相同质量的原混合物,得到固体质量为14.8g-m(O)=14.8g-0.2mol×16g/mol=11.6g,
故选A.
点评 本题考查混合物的计算,为高频考点,把握混合物中O元素质量的计算为解答的关键,侧重分析与计算能力的考查,注意CO还原混合物得到金属单质的混合物,题目难度不大.


 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案科目:高中化学 来源:2016-2017学年江西省高二上第一次月考化学试卷(解析版) 题型:选择题
下列说法正确的是
A.强酸跟强碱的反应热一定是中和热
B.1molC完全燃烧放热383.3kJ,其热化学方程为:C+O2=CO2 ΔH=-383.3kJ·mol-1
C.在稀溶液中,酸与碱发生中和反应生成1 mol H2O时的反应热叫做中和热
D.表示中和热的离子方程式为:H+(aq)+OH-(aq) H2O(l)ΔH=57.3KJ·mol-1
H2O(l)ΔH=57.3KJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧气是氧化产物 | |
| B. | 还原剂与氧化剂的物质的量之比为1:4 | |
| C. | 若生成4.48 L HF,则转移0.8 mol电子 | |
| D. | O2F2既是氧化剂又是还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
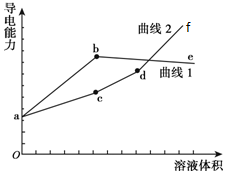 分别用浓度均为0.5mol/L NH3•H2O和NaOH溶液滴定20 mL 0.01mol/L Al2(SO4)3溶液,测得导电能力随溶液加入变化曲线如图所示,下列说法中正确的是( )
分别用浓度均为0.5mol/L NH3•H2O和NaOH溶液滴定20 mL 0.01mol/L Al2(SO4)3溶液,测得导电能力随溶液加入变化曲线如图所示,下列说法中正确的是( )| A. | 曲线1代表滴加NaOH溶液的变化曲线 | |
| B. | C点溶液中大量存在的离子是Na+和SO42- | |
| C. | b和d点对应的溶液均显酸性 | |
| D. | be段导电能力下降的原因是NH3•H2O?NH4++OH-,导致离子数目减少 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该溶液的PH大于1 | |
| B. | c(OH-)=c(H+)-C(CH3COO-) | |
| C. | 与等体积、等浓度的NaOH溶液完全中和后,溶液显中性 | |
| D. | 与足量锌反应比等体积、等浓度的盐酸反应速率慢,生成氢气的质量相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 6种 | B. | 7种 | C. | 8种 | D. | 9种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5种 | B. | 6种 | C. | 7种 | D. | 8种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学反应中,化学能全部转化为热能 | |
| B. | 已知C(s)+$\frac{1}{2}$O2(g)═CO(g),△H=-110.5kJ•mol-1,则碳的燃烧热为-110.5kJ•mol-1 | |
| C. | 测定中和热时,用铜制搅拌棒代替环形玻璃搅拌棒不影响测定结果 | |
| D. | 反应C(s)+CO2(g)═2CO(g)△H>0在较高温度下能自发进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 最高价含氧酸酸性:d>c>b | |
| B. | 它们均存在两种或两种以上的氧化物 | |
| C. | b与氢形成的化合物只存在极性共价键 | |
| D. | a、b、c的离子半径依次增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com