


科目:高中化学 来源:不详 题型:单选题
A.在100 ℃.101 kPa条件下,液态水的气化热为40.69 kJ·mol-1,则H2O(g) H2O(l) 的ΔH ="+" 40.69 kJ·mol-1 H2O(l) 的ΔH ="+" 40.69 kJ·mol-1 |
| B.已知MgCO3的Ksp = 6.82 × 10-6,则所有含有固体MgCO3的溶液中,都有c(Mg2+) = c(CO32-),且c(Mg2+) · c(CO32-)= 6.82 × 10-6 |
| C.常温下,在0.10 mol·L-1的NH3·H2O溶液中加入少量NH4Cl晶体,能使NH3·H2O的电离度降低,溶液的pH减小 |
| D.已知: |
| 共价键 | C-C | C=C | C-H | H-H |
| 键能/ kJ·mol-1 | 348 | 610 | 413 | 436 |
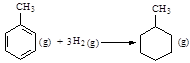 的ΔH为-384 kJ·mol-1
的ΔH为-384 kJ·mol-1查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2SO3(g) △H="-Q" kJ·mol-1(Q>0),测得SO2的转化率为90%,
2SO3(g) △H="-Q" kJ·mol-1(Q>0),测得SO2的转化率为90%,| A.1.8Q kJ | B.2Q kJ | C.Q kJ | D.0.9 QJ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.+283.5kJ·mol-1 | B.+172.5kJ·mol-1 |
| C.-172.5kJ·mol-1 | D.-504kJ·mol-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.2 L氟化氢气体分解成1 L氢气和1 L氟气吸收270 kJ热量 |
| B.1 mol氢气与1 mol氟气反应生成2 mol液态氟化氢放出热量小于270 kJ |
| C.在相同条件下,1 mol氢气与1 mol氟气的能量总和大于2 mol氟化氢气体的能量 |
| D.1个氢气分子与1个氟气分子反应生成2个氟化氢气体分子放出270 kJ的热量 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 C(s) =
C(s) =  CO2(g) + 2 Fe(s) ΔΗ="+234.1" kJ·mol-1
CO2(g) + 2 Fe(s) ΔΗ="+234.1" kJ·mol-1 O2(g) = Fe2O3(s) 的ΔΗ是:
O2(g) = Fe2O3(s) 的ΔΗ是:| A.-169.4kJ·mol-1 | B.-627.6 kJ·mol-1 |
| C.-744.7 kJ·mol-1 | D.-824.4 kJ·mol-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 与
与 反应过程中能量变化的曲线图。根据图像判断下列叙述中正确的是
反应过程中能量变化的曲线图。根据图像判断下列叙述中正确的是
A.该反应的热化学方程式为:N2(g)+3H2(g) 2NH3(g)ΔH=+92kJ/mol 2NH3(g)ΔH=+92kJ/mol |
B. 曲线是加入催化剂时的能量变化曲线 曲线是加入催化剂时的能量变化曲线 |
| C.加入催化剂,该化学反应的反应热数值会减小 |
D.反应2NH3(g)  N2(g)+3H2(g) ΔH=+92kJ/mol N2(g)+3H2(g) ΔH=+92kJ/mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题


 该反应的平衡常数表达式为 。
该反应的平衡常数表达式为 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.KOH(aq) + 1/2 H2SO4(aq) = 1/2K2SO4(aq) + H2O(l);ΔH =-11.46kJ/mol |
| B.2KOH(s) + H2SO4(aq) = K2SO4(aq) + 2H2O(l);ΔH =-114.6kJ/mol |
| C.2KOH(aq) + H2SO4 =K2SO4(aq) + H2O(l);ΔH =+114.6kJ/mol |
| D.KOH (aq) + 1/2 H2SO4(aq) = 1/2K2SO4(aq) + H2O(l);ΔH =-57.3kJ/mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com