
下列各组物质能相互反应得到Al(OH)3的是( )
A.Al跟NaOH溶液共热
B.少量Al(NO3)3跟大量的NaOH溶液
C.Al2O3和水共热
D.Al2(SO4)3和过量的氨水
 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:
判断下列说法是否正确
(1)1 mol O2的质量是32 g·mol-1( )
(2)H2的摩尔质量是2 g( )
(3)对原子而言,摩尔质量就是相对原子质量( )
查看答案和解析>>
科目:高中化学 来源: 题型:
用地壳中某主要元素生产的多种产品在现代高科技中占有重要位置,足见化学对现代物质文明的重要作用。例如:
(1)计算机芯片的主要成分是________。
(2)光导纤维的主要成分是________。
(3)目前应用最多的太阳能电池的光电转化材料是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某无色透明溶液,跟金属铝反应放出H2,试判断下列离子:
Mg2+、Ba2+、Cu2+、H+、Ag+、SO 、SO
、SO 、OH-、HCO
、OH-、HCO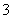 、NO
、NO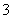 ,何种离子能大量存在于此溶液中。
,何种离子能大量存在于此溶液中。
(1)当生成Al3+时,可能存在_________________________________。
(2)当生成[Al(OH)4]-时,可能存在________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
纯铁的熔点为1 535 ℃,而高炉中炼铁时生铁(含碳量较高的铁的合金)在1 200 ℃左右就熔化了,这是因为( )
A.铁的纯度越高熔点越低
B.合金的熔点比其成分物质的熔点高
C.因为形成了铁碳合金,所以熔点变低
D.生铁在高炉内熔化的过程中发生了化学反应
查看答案和解析>>
科目:高中化学 来源: 题型:
将8 g铁片放入100 mL CuSO4溶液中,当溶液中Cu2+全部被还原时,“铁片”的质量变为8.2 g,则原CuSO4溶液的物质的量浓度为__________________,发生反应的离子方程式为________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
普通玻璃、钢铁和玻璃钢是三种不同的材料,它们在性能方面差别很大。请根据学过的知识,回答下面问题。
(1)普通玻璃的成分是____________________________________________。
(2)铁在人类的生产和生活中有着十分重要的应用。铁的应用,经历了________到________到________的演变过程。
(3)某种复合材料具有耐高温、强度高、导电性好、导热性好的特点,估计该复合材料的基体和增强体材料可能分别是( )
A.金属;碳纤维 B.陶瓷;SiO2
C.合成树脂;SiO2、Al2O3、MgO D.合成树脂;碳纤维
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com