
【题目】随着核电荷数的递增,氧化性逐渐减弱的一组是( )
A.I2、Br2、Cl2、F2B.F2、Cl2、Br2、I2C.F-、Cl-、Br-、I-D.Li、Na、K、Rb
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案科目:高中化学 来源: 题型:
【题目】根据如图所示实验装置,回答下列问题:
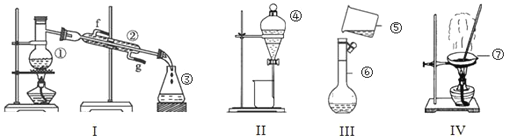
(1)写出下列仪器的名称:②_________,③_________,⑦__________。
(2)上述仪器中实验之前需检查装置是否会漏水的是______________(填仪器名称)。
(3)实验室准备用18mol/L浓硫酸配制100mL 3mol/L稀硫酸,则所需浓硫酸的体积是____mL(保留一位小数),量取浓硫酸所用量筒的规格是____(选填“10mL”、“25mL”或“50mL”)。在实验操作的摇匀过程中,不慎洒出几滴,此时应采取的措施是_______,若所配制的稀硫酸浓度偏大,则下列可能的原因分析中正确的是_______。
A.配制前,容量瓶中有少量蒸馏水 B.量取浓硫酸时,仰视液体的凹液面
C.未冷却,立即转移至容量瓶定容 D.定容时,俯视溶液的凹液面
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na2S2O3·5H2O常用作冲洗照相底片的定影剂,实验室以Na2S、Na2CO3、SO2为原料,利用下图装置可制取少量Na2S2O3·5H2O,其实验原理为Na2CO3+SO2=Na2S2O3+CO2;2Na2S+3SO2==2Na2SO3+3S;Na2SO3+S=Na2S2O3。回答下列问题:
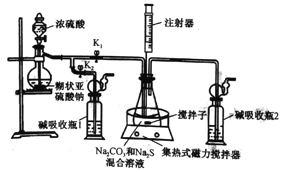
(1)打开K1,关闭K2,将锥形瓶中的溶液加热至35℃,打开滴液漏斗活塞慢慢滴加浓硫酸,锥形瓶中的现象是: ①导管口有气泡冒出;②__________________。
(2)通过注射器取样,监控锥形瓶中溶液pH=7~8,锥形瓶中酸性不能过强的原因是_______。当锥形瓶中溶液的pH接近7时,应进行的操作是__________________________。
(3)反应结束后将锥形瓶中混合液经如下处理可Na2S2O3·5H2O粗晶体:
![]()
①趁热过滤的目的是______________________。
②粗晶体中含有Na2CO3、Na2SO3、Na2SO4等杂质,利用下列提供的试剂,检验粗产品中含有Na2CO3。
可选试剂: a.品红溶液 b.酸性高锰酸钾溶液 c.澄清石灰水 d.NaOH溶液 e.稀硫酸
实验方案:取适量所得粗晶体配成溶液,滴加足量的稀硫酸,将产生的气体依次通过酸性高锰酸钾溶液、_____(填试剂序号)、澄清石灰水,若______(填现象),则证明产品中含有Na2CO3。
(4)粗晶体中Na2S2O3·5H2O质量分数的测定:称取2.500g粗晶体溶于水,配成100mL溶液,取25.00mL溶液于锥形瓶中,用0.4000 mol/L的酸性高锰酸钾标准溶液滴定,消耗标准溶液的体积为10.00mL,Na2S2O3·5H2O的质量分数为______ (忽略杂质对滴定的影响;S2O32-被酸性高锰酸钾溶液氧化为SO42-)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇是一种重要的化工原料,工业上可用CO和H2合成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g) ![]() CH3OH(g) ΔH = -90.8 kJ·mol-1
CH3OH(g) ΔH = -90.8 kJ·mol-1
(1)某研究小组,在温度和容器的容积保持不变时,研究该反应是否达到平衡状态,以下五位同学对平衡状态的描述正确的是__________。
A.甲:H2的消耗速率等于CH3OH的生成速率
B.乙:容器内的压强保持不变
C.丙:容器内气体的密度保持不变
D.丁:容器中气体的平均摩尔质量保持不变
(2)若在一定温度下、容积为2L的密闭容器中,投入2 mol CO、4 mol H2,保持恒温、恒容,测得反应达到平衡时H2转化率为75%,求平衡时CH3OH的浓度=__________mol/L
(3)已知在298K、101kPa下:甲醇的燃烧热化学方程式为:
CH3OH(l)+ 3/2 O2(g)= CO2(g)+ 2H2O(l) ΔH= -725.8 kJ·mol-1;
CO的燃烧热化学方程式为:CO(g)+ 1/2 O2(g)= CO2(g) ΔH= -283 kJ·mol-1;
H2O (g) === H2O(l) ΔH= -44 kJ·mol-1
请写出甲醇不完全燃烧生成一氧化碳和水蒸气的热化学方程式__________。
(4)以甲醇为燃料,氧气为氧化剂,KOH溶液为电解质溶液,可制成燃料电池(电极材料为惰性电极)
①该电池中通入甲醇的是电源的__________(填正、负)极,若KOH溶液足量,则写出电池总反应的离子方程式__________。
②若电解质溶液中KOH的物质的量为0.5mol,当有0.5mol甲醇参与反应时,产物恰好为KHCO3时,该电池的负极反应式为__________,所得溶液中各种离子的物质的量浓度由大到小的顺序是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“长征二号”系列火箭用的燃料是液态的偏二甲肼(C2H8N2),氧化剂是液态的N2O4,已知1.5 g偏二甲肼完全燃烧生成N2、CO2和液态H2O放出热量50 kJ。下列说法不正确的是( )。
A.燃料在火箭发动机中燃烧主要是将化学能转化为热能和机械能
B.偏二甲肼在N2O4中的燃烧反应是放热反应
C.该反应中偏二甲肼和N2O4总能量低于CO2、N2和H2O的总能量
D.偏二甲肼在N2O4中燃烧的化学方程式为C2H8N2+2N2O4![]() 2CO2+3N2+4H2O
2CO2+3N2+4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学中有许多物质之间的反应符合下列关系图,图中其他产物及反应所需条件均已略去。
![]()
![]()
![]()
![]()
![]()
![]()
![]()
对于上图的变化下列判断不正确的是( )
A. 当A是正盐、X是强酸时,D可能是酸性氧化物
B. 当X是强碱溶液时,B一定是NH3
C. B可能是单质
D. D可能是一种酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中国药学家屠呦呦因发现青蒿素及其抗疟疗效,荣获诺贝尔生理学或医学奖。青蒿素结构式如右图所示,下列有关青蒿素研究的说法不正确的是
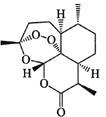
A. 提取过程为防止破坏青蒿素结构应避免高温,故用低沸点溶剂乙醚进行萃取
B. 可使用红外光谱测出这个分子的相对分子质量,也可用质谱仪确定这个分子的环状结构
C. 青蒿素是脂溶性的,既可看作是醚类也可看作是酯类化合物,既有氧化性又有还原性
D. 元素分析仪可以确定青蒿素中是否含有C、H、O等元素
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com