
| A. | 向氨水中加水可使溶液中n(H+)和n(OH-)均增大 | |
| B. | 若Na2A、Na2B溶液的pH分别为8和9,则酸性一定是H2A>H2B | |
| C. | 已知室温时,0.1mol•1-1某一元酸HA的电离平衡常数为1×10-7,则该酸的电离度约为0.1% | |
| D. | 新制氯水中:c(H+)>c(Cl-)>c(CLO-)>c(OH-) |
分析 A、氨水中存在电离平衡NH3•H2O?NH4++OH-,加水促进氨水的电离;
B、Na2A、Na2B溶液的浓度没有说明无法判断H2A,H2B的酸性强弱;
C、电离平衡常数=$\frac{c({A}^{-}).c({H}^{+})}{c(HA)}$=1×10-2,则c(H+)=$\sqrt{1{0}^{-7}×0.1}$=10-4mol/L,电离度=$\frac{c(HA)(电离)}{c(HA)(总)}$×100%;
D、氯水中存在HCl和HClO,HCl完全电离,HClO部分电离.
解答 解:A、氨水中存在电离平衡NH3•H2O?NH4++OH-,加水促进氨水的电离,电离平衡向正方向移动,n(H+)和n(OH-)均增大,故A正确;
B、Na2A、Na2B溶液的浓度没有说明无法判断H2A,H2B的酸性强弱,故B错误;
C、电离平衡常数=$\frac{c({A}^{-}).c({H}^{+})}{c(HA)}$=1×10-7,则c(H+)=$\sqrt{1{0}^{-7}×0.1}$=10-4mol/L,电离度=$\frac{c(HA)(电离)}{c(HA)(总)}$×100%=$\frac{1{0}^{-4}mol/L}{0.1mol/L}$=0.1%,故C正确;
D、氯水中存在HCl和HClO,HCl完全电离,HClO部分电离,所以溶液:c(H+)>c(Cl-)>c(CLO-)>c(OH-),故D正确.
故选B.
点评 本题考查了电离平衡移动的影响因素、电解质溶液中离子浓度大小比较、离子积常数的计算应用和溶液PH计算分析,掌握基础是关键,题目较简单.


科目:高中化学 来源: 题型:选择题
| A. | 一定含有Mg2+、Al3+、Clˉ,不含Na+、NH4+ | |
| B. | 一定含有Na+、Mg2+、Clˉ,不含NH4+,可能含有Al3+ | |
| C. | c(Clˉ)为 4.00mol•L-1,c(Al3+)为1.00 mol•L-1 | |
| D. | c(Mg2+)为 1.00mol•L-1,c(Na+)为 0.50 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | LiH与D2O反应,所得氢气的摩尔质量为4g/mol | |
| B. | 1mol LiAlH4在125℃完全分解,转移3mol电子 | |
| C. | LiH与水反应的化学方程式为:LiH+H2O=LiOH+H2↑ | |
| D. | LiH与中微粒半径r(Li+)>r(H-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 第一电离能大小:S>P>Si | |
| B. | 电负性顺序:C<N<O<F | |
| C. | 因为晶格能CaO比KCl高,所以KCl比CaO熔点高 | |
| D. | SO2与CO2化学性质类似,分子结构也都呈直线型,相同条件下SO2的溶解度更大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 0℃ | 50℃ | 80℃ | |
| Ca(OH)2 | 0.173g | 0.13g | 0.094g |
| Ba(OH)2•8H2O | 1.64g | 13.2g | 101.4g |
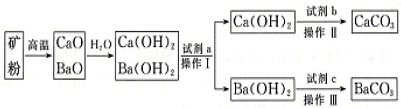
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 时间/min | CO | H2O(g) | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | 0.100 | 0.200 | 0.100 | 0.100 |
| 4 | 0.100 | 0.200 | 0.100 | 0.100 |
| 5 | 0.116 | 0.216 | 0.084 | C1 |
| 6 | 0.096 | 0.266 | 0.104 | C2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,48gO2和O3含有的氧原子数均为3NA5.4g铝与足量NaOH反应转移的电子数为0.3NA | |
| B. | 12g重水(D2O)中含有的电子数为6 NA | |
| C. | 标准状况下,11.2L苯所含原子数为6NA | |
| D. | 160g胆矾溶于水形成1L溶液,溶液的物质的量浓度为1mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com