
【题目】下列离子方程式正确的是( )
A. 氯化铁腐蚀铜板:Fe3++Cu===Fe2++Cu2+
B. 实验室制氯气:MnO2+4HCl(浓)![]() Mn2++2Cl2↑+2H2O
Mn2++2Cl2↑+2H2O
C. 稀硫酸中加氢氧化钡溶液至溶液呈中性:Ba2++H++OH-+SO![]() ===BaSO4↓+H2O
===BaSO4↓+H2O
D. 用氢氧化钠溶液吸收少量二氧化硫:2OH-+SO2 ===SO![]() +H2O
+H2O
科目:高中化学 来源: 题型:
【题目】Sn元素位于元素周期表第IVA族,SnCl4可用作媒染剂和催化剂,工业上常用氯气与金属锡在300℃反应制备SnCl4。SnCl4极易水解,SnCl2、SnCl4的一些物理数据如下:
物质 | 状态 | 熔点/X; | 沸点/X; |
Sn | 银白色固体 | 232 | 2 260 |
SnCl2 | 无色晶体 | 246 | 652 |
SnCl4 | 无色液体 | -33 | 114 |
用下列装置合成四氯化锡(夹持装置略)。
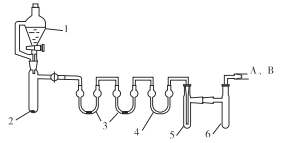
注:仪器3中各加入0.6 mL浓硫酸
实验操作如下:
a.把干燥的仪器按图示装置连接好,在仪器1中加入8 mL浓盐酸,在仪器2中加入1.0 g KClO3,在仪器5中加入2~3颗Sn粒;
b.打开活塞,让盐酸流下,均匀产生Cl2并充满整套装置,然后加热Sn粒,将生成的SnCl4收集在仪器 6中;
c.Sn粒反应完毕后,停止加热,同时停止滴加盐酸,取下仪器6,迅速盖好盖子。
请回答:
(1)仪器1的名称是___________。
(2)下列说法不正确的是______。
A.装置连接好,加入药品前要检査装置的气密性
B.产生的Cl2先充满整套装置,这步操作不可以省略
C.操作中应控制盐酸的滴入速率,不能太快,也不能太慢
D.仪器6可用冰水浴冷却,也可以自然冷却
(3)仪器6后还应连接A、B装置,A装置的作用是_____________。
(4)已知SnCl2易水解,易氧化,且还原性:Sn2+>I-,SnCl4氧化性弱。有关SnCl4和SnCl2的说法不正确的是_________。
A.实验室配制SnCl2溶液时,除加入盐酸外,还应加入锡粒
B.将产品溶于盐酸,可用溴水检测,若溴水橙色褪去,说明SnCl4中含有SnCl2
C. SnCl4在空气中与水蒸气反应生成白色SnO2·xH2O固体,只看到有白烟现象,化学方程式为SnCl4+(x+2)H2O=SnO2·xH2O+4HC1
(5)经测定产品中含冇少量的SnCl2,可能的原因(用化学方程式表示):_______________。
(6)产品中含少量SnCl2,测定SnCl4纯度的方法:取0.200 g产品溶于50 mL的稀盐酸中,加入淀粉溶液 作指示剂,用0.0100mol/L碘酸钾标准溶液滴定至终点,消耗标准液4.00 mL,反应原理为:3 SnCl2+KIO3+6HC1=3SnCl4+KI+3H2O,判断滴定终点的依据为_______,产品的纯度为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由几种离子化合物组成的混合物,含有以下离子中的若干种:K+、 NH4+、 Mg2+、 Ba2+、 Cl-、 SO42—、 CO32—。
将该混合物溶于水后得澄清溶液。 现取3份100 mL该溶液分别进行如下实验:
实验序号 | 实验内容 | 实验结果 |
A | 加 AgNO3溶液 | 有白色沉淀生成 |
B | 加足量 NaOH 溶液并加热 | 收集到气体 1.12 L(标准状况下) |
C | 加足量 BaCl2溶液,对所得沉淀进行洗涤、干燥、称量;再向沉淀中加足量稀盐酸,然后干燥称量 | 第一次称量沉淀质量为6.63 g,第二次称量沉淀质量为4.66 g |
试回答下列问题:
(1)根据实验A判断 Cl-是否存在_____(填“一定存在” 、 “一定不存在” 或“不能确定”)。
(2)该混合物中一定不存在的离子是_____。
(3)写出实验B发生反应的离子方程式_____________。
(4)溶液中一定存在的阴离子及其物质的量浓度为(可不填满):
阴离子符号 | 物质的量浓度(mol·L-1) |
(5)混合物中是否存在 K+?_____(填“存在” 或“不存在” )
①如果存在, c(K+) _____mol/L(如果选择“不存在” ,此问不必做答)
②如果不存在,判断的理由是_____。(如果选择“存在” ,此问不必做答)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A﹒现有CO、CO2、O3三种气体,它们分别都含有1 mol O,则三种气体的物质的量之比为3∶2∶1
B﹒n g Cl2中有m个Cl原子,则阿伏加德罗常数NA的数值可表示为35.5m/n
C﹒标准状况下,11.2 L X气体分子的质量为16 g,则X气体的摩尔质量是32
D﹒5.6 g CO和4.48 L CO2中含有的碳原子数一定相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在指定的溶液中一定能大量共存的是
A. 漂白粉的水溶液中: Fe2+、K+ 、Ca2+、Br-
B. pH=0的溶液中:Cu2+、Cl-、SO![]() 、Na+
、Na+
C. 含大量NO3-的溶液:Fe3+、Al3+、SO32-、H+
D. 能够与金属Al常温下反应放出气体的溶液:HCO![]() 、Na+、Ca2+、Cl-
、Na+、Ca2+、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由14CO和12CO组成的混合气与同温同压下空气(平均相对分子质量为29)的密度相同,则下列关系正确的是
A. 混合气中14CO与12CO的分子数之比为14︰15
B. 混合气中14CO与12CO的物质的量之比为1︰1
C. 混合气中14CO与12CO的质量之比为14︰15
D. 混合气中14CO与12CO的密度之比为1︰1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关,下列说法错误的是
A. 明矾可用作净水剂
B. 纯碱可用于中和过多的胃酸
C. 硫酸铜常用作游泳馆池水消毒剂
D. 硫酸钡可用于胃肠X射线造影检查
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计如下实验方案,以分离NaCl和BaCl2两种固体混合物,回答下列问题:

供选试剂:Na 2CO3溶液、Na2SO4溶液、K2CO3溶液、K2SO4溶液、盐酸
(1)操作②的名称是______________。
(2)试剂a是________(填化学式,下同),试剂b是____________,固体B是________。
(3)加入试剂a所发生的化学反应方程式为______________________________________。
(4)简述操作③洗涤沉淀的操作步骤_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:①CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH1=Q1
②H2(g)+![]() O2(g)===H2O(g) ΔH2=Q2
O2(g)===H2O(g) ΔH2=Q2
③H2(g)+![]() O2(g)===H2O(l) ΔH3=Q3
O2(g)===H2O(l) ΔH3=Q3
常温下取体积比为4∶1的甲烷和氢气的混合气体11.2 L(已折合成标准状况)经完全燃烧恢复到常温,放出的热量为
A.0.4Q1+0.05Q2 B.0.4Q1+0.1Q2
C.0.4Q1+0.05Q3 D.0.4Q1+0.1Q3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com