
【题目】下表中如图所示的一些物质或概念间的从属关系,不正确的是
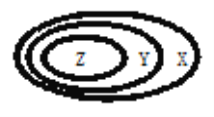
Z | Y | X | |
A | 氧化物 | 化合物 | 纯净物 |
B | 非电解质 | 电解质 | 化合物 |
C | 胶体 | 分散系 | 混合物 |
D | 碱性氧化物 | 金属氧化物 | 氧化物 |
A.AB.BC.CD.D
 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案 初中暑期衔接系列答案
初中暑期衔接系列答案科目:高中化学 来源: 题型:
【题目】
近年来,随着聚酯工业的快速发展,氯气的需求量和氯化氢的产出量也随之迅速增长。因此,将氯化氢转化为氯气的技术成为科学研究的热点。回答下列问题:
(1)Deacon发明的直接氧化法为:4HCl(g)+O2(g)=2Cl2(g)+2H2O(g)。下图为刚性容器中,进料浓度比c(HCl) ∶c(O2)分别等于1∶1、4∶1、7∶1时HCl平衡转化率随温度变化的关系:
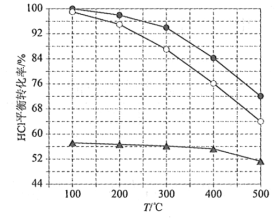
可知反应平衡常数K(300℃)____________K(400℃)(填“大于”或“小于”)。设HCl初始浓度为c0,根据进料浓度比c(HCl)∶c(O2)=1∶1的数据计算K(400℃)=____________(列出计算式)。按化学计量比进料可以保持反应物高转化率,同时降低产物分离的能耗。进料浓度比c(HCl)∶c(O2)过低、过高的不利影响分别是____________。
(2)Deacon直接氧化法可按下列催化过程进行:
CuCl2(s)=CuCl(s)+![]() Cl2(g) ΔH1=83 kJ·mol-1
Cl2(g) ΔH1=83 kJ·mol-1
CuCl(s)+![]() O2(g)=CuO(s)+
O2(g)=CuO(s)+![]() Cl2(g) ΔH2=-20 kJ·mol-1
Cl2(g) ΔH2=-20 kJ·mol-1
CuO(s)+2HCl(g)=CuCl2(s)+H2O(g) ΔH3=-121 kJ·mol-1
则4HCl(g)+O2(g)=2Cl2(g)+2H2O(g)的ΔH=_________ kJ·mol-1。
(3)在一定温度的条件下,进一步提高HCI的转化率的方法是______________。(写出2种)
(4)在传统的电解氯化氢回收氯气技术的基础上,科学家最近采用碳基电极材料设计了一种新的工艺方案,主要包括电化学过程和化学过程,如下图所示:
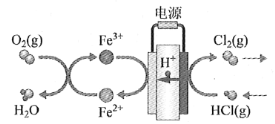
负极区发生的反应有____________________(写反应方程式)。电路中转移1 mol电子,需消耗氧气__________L(标准状况)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~G是前四周期除稀有气体之外原子序数依次增大的七种元素。A与其他元素既不同周期又不同族;B、C的价电子层中未成对电子数都是2;E核外的s、p能级的电子总数相等;F与E同周期且第一电离能比E小;G的+1价离子(G+)的各层电子全充满。回答下列问题:
(1)写出元素名称:B_______,G_______。
(2)写出F的价电子排布图:_______。
(3)写出化合物BC的结构式:__________________。
(4)由A、C、F三元素形成的离子[F(CA)4]— 是F在水溶液中的一种存在形式,其中F的杂化类型是________________。
(5)在测定A、D形成的化合物的相对分子质量时,实验测定值一般高于理论值的主要原因是______________________。
(6)E的一种晶体结构如图甲,则其一个晶胞中含有_______个E;G与D形成的化合物的晶胞结构如图乙,若晶体密度为ag/cm3,则G与D最近的距离为____pm
(阿伏加德罗常数用NA表示,列出计算表达式,不用化简;乙中○为G,●为D。)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求填空(所涉及元素均为前20号)
(1)A元素的原子M层有5个电子,则其原子结构示意图为__________________;最高价氯化物的化学式_______________________。
(2)C元素原子最外层电子是最内层电子的3倍,其形成的离子与Ar元素有相同的电子结构,请写出C离子的结构示意图和电子式:________________、_________。
(3)标出下列反应的电子转移方向和数目,并填写有关内容:
KClO3+6HCl→3Cl2↑+3H2O+KCl、___________
氧化剂______________;氧化产物______________;还原剂______________;还原产物______________;被氧化的元素______________;HCl的作用______________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组欲测定室温下(25℃,101kPa)的气体摩尔体积,请回答以下问题。该小组设计的简易实验装置如图所示:

该实验的主要操作步骤如下:
①配制 100 mL 1.0mol/L的盐酸溶液:.
②用_______________(填仪器名称并注明规格)量取7.5mL 1.0mol/L的盐酸溶液加入锥形瓶中;
③称取ag已除去表面氧化膜的镁条,并系于铜丝未端,为使HCl全部参加反应,a的数值至少为__________;
④往广口瓶中装入足量水,按上图连接好装置,检查装置的气密性;
⑤反应结束后待体系温度恢复到室温,忽略导管中的水,读出量筒中水的体积为91.9mL
请将上述步骤补充完整并回答下列问题。
(1)步骤①中所需要带刻度的仪器为__________,若用36.5%的浓盐酸(密度为1.20g/mL)
进行稀释配制,则需要量取该浓盐酸___________mL
(2)步骤①中,配制100 mL 1.0mol/L的盐酸溶液时,下列哪些操作会使配制浓度偏低___________(填写字母).
A.用量筒量取浓盐酸时,俯视量筒的刻度
B.容量瓶未干燥即用来配制溶液.
C.未洗涤烧杯和玻璃棒
D.定容完成后,将容量瓶倒置摇匀后;发现液面低于刻度线
E.在容量瓶中定容时俯视容量瓶刻度线.
F.烧杯中有少量水.
(3)请填写操作步骤中的空格:步骤②_________步骤③_______________
(4)实验步骤5中应选用______________(填字母)的量筒。.'
A.100 mL B.200mL C.500mL
(5)忽略水蒸气影响,在该条件下测得气体摩尔体积为Vm=_____________L/mol(保留2位小数)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W是原子序数依次增大的短周期主族元素,且离子具有相同的电子层结构。X的一种单质可杀菌消毒。W原子的最外层电子数与最内层电子数相等。下列说法不正确的是
A. 原子半径r(Z)>r(W)>r(X)>r(Y)
B. X的简单氢化物热稳定性比Y的强
C. 四种元素常见单质中,Y2的氧化性最强
D. X能与Z形成Z2X2,该化合物中含离子健和非极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关晶体的结构如图所示,下列说法中不正确的是 ( )


A. 在NaCl晶体中,距Na+最近的Cl-形成正八面体
B. 在CaF2晶体中,每个晶胞平均占有4个Ca2+
C. 在金刚石晶体中,碳原子与碳碳键个数的比为1∶2
D. 该气态团簇分子的分子式为EF或FE
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)向25mL沸水中逐滴加入5~6滴FeCl3饱和溶液;继续煮沸至溶液呈红褐色,停止加热可以制取Fe(OH)3胶体。试回答下列问题:
①写出此过程中的化学方程式:__;
②向所得Fe(OH)3胶体中逐滴滴加硫酸溶液,开始产生红褐色沉淀,继续滴加,沉淀最终消失且得棕黄色溶液,写出相关的离子方程式___;
(2)鸡蛋的内膜是一种半透膜,某同学拟用这种半透膜进行除去淀粉溶液中所含食盐的实验。设计步骤如下:
a.把鸡蛋的一头敲破,倒出蛋清、蛋黄,洗净蛋膜内部,将另一头浸泡在稀酸中溶去部分蛋壳(中间的蛋壳留着,起固定作用);
b.在一只小烧杯中加入适量蒸馏水,将洗净了蛋膜外部的蛋壳架在小烧杯上,蛋膜浸入蒸馏水中(如图);
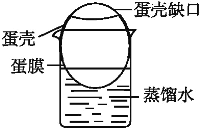
c.向蛋膜内加入淀粉和食盐的混合溶液,静置一段时间;
d.拿走蛋膜,检验烧杯中有无淀粉和食盐。
根据以上叙述,回答下列问题:
①步骤a中溶解蛋壳(主要成分为CaCO3)的酸最好是_____(填“盐酸”“硫酸”或“醋酸”)。
②检验烧杯中有无淀粉,操作是_____,检验烧杯中有无NaCl,操作是_____。
③为尽可能除去淀粉溶液里的食盐,可采取的措施是______(填入正确选项前的字母)。
A.换大烧杯,用大量水进行渗析
B.多次渗析,每次用水量不要太多
C.将蛋膜放在有流水的水槽中进行渗析
④如何证明淀粉溶液中的食盐有没有全部除去?简述实验过程:_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应mA(s)+nB(g)![]() eC(g)+fD(g),反应过程中,当其他条件不变时,C的体积分数ψ(C)在不同温度和不同压强的条件下随时间的变化如图所示。
eC(g)+fD(g),反应过程中,当其他条件不变时,C的体积分数ψ(C)在不同温度和不同压强的条件下随时间的变化如图所示。
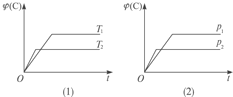
下列叙述正确的是()
A. 平衡后,若使用催化剂,C的体积分数增大
B. 平衡后,若温度升高,化学平衡向正反应方向移动
C. 化学方程式中,化学计量数的关系为n<e+f
D. 平衡后,增加A的质量,化学平衡向正反应方向移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com