
【题目】【化学—选修3:物质结构与性质】我国科学家借助自主研制的新型钨钴合金催化剂攻克了单壁碳纳米管结构的可控制备难题。
(1)基态钴原子的核外电子排布式为 。单壁碳纳米管可看作石墨烯沿一定方向卷曲而成的空心圆柱体,其碳原子的杂化方式为 。
(2)纳米结构氧化钴可在室温下将甲醛(HCHO)完全催化氧化,已知甲醛各原子均满足稳定结构,甲醛分子属 分子(选填“极性”“非极性”),其立体构型为 。
(3)橙红色晶体羰基钴[Co2(CO)8]的熔点为52℃,可溶于多数有机溶剂。该晶体属于 晶体,三种元素电负性由大到小的顺序为(填元素符号) 。配体CO中σ键与π键数之比是 。

(4)元素铁、钴、镍并称铁系元素,性质具有相似性。某含镍化合物结构如上图所示,分子内的作用力不可能含有 (填序号)。
A离子键 B共价键 C金属键 D配位键 E氢键
(5)钨为熔点最高的金属,硬度极大,其晶胞结构如图所示,已知钨的密度为ρ g·cm-3,则每个钨原子的半径r= cm。(只需列出计算式)

【答案】(1)[Ar]3d74s2(1分);sp2(1分);
(2)极性(1分);平面三角形(1分);
(3)分子(1分);O>C>Co(2分);1∶2(2分);
(4)AC(3分);(5)![]() ×
×![]() (3分)
(3分)
【解析】
试题分析:(1)Co的原子序数是27,则其基态钴原子的核外电子排布式为[Ar]3d74s2。单壁碳纳米管可看作石墨烯沿一定方向卷曲而成的空心圆柱体,其碳原子的杂化方式与石墨中的相同,为sp2。
(2)已知甲醛各原子均满足稳定结构,其立体构型为平面三角形,但由于价格不对称,所以甲醛分子属极性分子。(3)橙红色晶体羰基钴[Co2(CO)8]的熔点为52℃,可溶于多数有机溶剂,这说明该晶体属于分子晶体。非金属性越强,电负性越大,因此三种元素电负性由大到小的顺序为O>C>Co。CO的结构和氮气相类似,所以配体CO中σ键与π键数之比是1∶2。
(4)根据结构示意图可知分子中存在共价键、配位键和氢键,但不能存在金属键和离子键,答案选AC。(5)根据钨晶胞结构图可知晶胞中含有1+8×1/8=2个原子。已知钨的密度为ρ g·cm-3,则晶胞的体积是![]() ,则晶胞的边长是
,则晶胞的边长是![]() ,因此每个钨原子的半径r=
,因此每个钨原子的半径r=![]() ×
×![]() cm。
cm。


科目:高中化学 来源: 题型:
【题目】将4体积的H2和1体积的O2混合,4 g这种混合气体在标准状况下所占的体积是
A. 5.6 L B. 11.2 L C. 22.4 L D. 33.6 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各物质中的少量杂质,可用括号内的试剂和方法除去的是
A.苯中溶有苯酚(浓溴水,过滤) B.甲烷中含有乙烯(溴水,洗气)
C.溴苯中溶有溴(苯,分液) D.乙醇中含有水(金属钠,蒸馏)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上利用硫铁矿烧渣(主要成分为Fe3O4、Fe2O3、FeO、SiO2)制备铁红(Fe2O3)的生产流程如下:
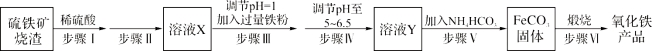
试回答下列问题:
(1)步骤Ⅰ所得溶液中铁元素的化合价是 。
(2)实验室中实现步骤Ⅱ中分离操作需要的仪器有 、铁架台、玻璃棒、烧杯。
(3)步骤Ⅲ中发生的离子方程式 ,向反应后的溶液中加入试剂 ,当观察到 说明步骤Ⅲ已经进行完全。
(4)步骤Ⅳ中不能选用试剂 调节溶液的pH(填字母编号)。
a.FeO固体 b.氢氧化钠溶液 c.Fe2O3固体 d.氨水
(5)室温下FeCO3达到溶解平衡时溶液pH=8.5,c(Fe2+)=1.2×10-6 mol·L-1。则FeCO3固体产物中 (选填“有”或“无”)Fe(OH)2。(已知:Ksp[Fe(OH)2]=4.8×10-16)
(6)步骤Ⅵ中发生反应的化学反应方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于胶体和溶液的叙述中正确的是
A. 胶体带电荷,而溶液呈电中性
B. 胶体加入电解质可产生沉淀,而溶液不能
C. 胶体是一种介稳性的分散系,而溶液是一种非常稳定的分散系
D. 胶体和溶液都能够产生丁达尔效应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.浓硫酸具有强氧化性,稀硫酸无氧化性
B.浓硫酸在常温下可迅速与铜片反应放出二氧化硫气体
C.浓硫酸在常温下能够使铁、铝形成氧化膜而钝化
D.浓硫酸是一种干燥剂,能够干燥氨气、氢气等气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于苯酚的叙述中,正确的是
A.呈弱酸性,使石蕊试液显浅红色 B.分子中的13个原子有可能处于同一平面
C.可以和NaHCO3溶液反应产生气体 D.能与FeCl3溶液反应生成紫色沉淀a
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值。下列说法正确的是
A. 将2 mol NO和2 mol O2混合,充分反应后体系中原子总数为8NA
B. 将100 mL 0.1 mol·L﹣1的FeCl3溶液滴入沸水中可制得Fe(OH)3胶粒0.01NA
C. CO2通过Na2O2使其增重a g时,反应中转移的电子数为![]() NA
NA
D. 100 g质量分数为9.8%的H2SO4水溶液中含氧原子数目为0.4NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com