
已知Ba(AlO2)2可溶于水。下图表示的是向含A12(SO4)3 0.01mol的溶液中逐滴加入Ba(OH)2溶液时,生成沉淀的物质的量y与加入Ba(OH)2的物质的量x的关系(其中a、c分别是0b段和bd段的中点)。下列有关叙述正确的是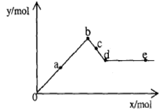
| A.a时沉淀的质量为3.495 g |
| B.b时沉淀的物质的量为0.05 mol |
| C.c时溶液中Ba2+离子的物质的量为0.005 mol |
| D.e时溶液中AlO2—的物质的量为0.01 mol |
BC
解析试题分析:硫酸铝和氢氧化钡反应的方程式是Al2(SO4)3+3Ba(OH)2=2Al(OH)3↓+3BaSO4↓,如果继续加入氢氧化钡,则氢氧化铝开始溶解,反应的化学方程式是2Al(OH)3+Ba(OH)2=Ba(AlO2)2+4H2O。由于a、c分别是0b段和bd段的中点,所以a点生成0.01mol氢氧化铝和0.015mol硫酸钡,质量之和是3.495g+0.78g=4.275g,A不正确;b时沉淀是0.02mol氢氧化铝和0.03mol硫酸钡,其物质的量之和为0.05 mol,B正确;c点有0.01mol氢氧化铝溶解,生成0.005mol Ba(AlO2)2,此时溶液中Ba2+离子的物质的量为0.005 mol,C正确;e点溶液中的沉淀只有硫酸钡,氢氧化铝完全溶解,则溶液中AlO2—的物质的量为0.02mol,D不正确,答案选BC。
考点:考查硫酸铝和氢氧化钡反应的有关计算
点评:该题是高考中的常见题型,属于综合性试题的考查,侧重对学生解题能力的培养。试题综合性强,贴近高考,旨在培养学生分析、归纳、总结问题的能力。有利于调动学生的学习兴趣和学习积极性,也有助于培养学生的逻辑推理能力和抽象思维能力。该题的关键是明确反应原理,然后结合题意和图像灵活运用即可。


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
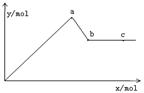
(4分)已知Ba(AlO2)2可溶于水。右图表示的是向KA1(SO4)2溶液中逐滴加入Ba(OH)2溶液时,生成沉淀的物质的量y与加入Ba(OH)2的物质的量x的关系。完成下列问题:
(1)a点时反应的离子方程式是
(2)a、b两点消耗Ba(OH)2的物质的量之比是
查看答案和解析>>
科目:高中化学 来源:2013届河北省衡水中学高三第三次模拟考试化学试卷(带解析) 题型:单选题
已知Ba(AlO2)2可溶于水,向含有1 mol Al2(SO4)3的溶液中加入含有b mol Ba(OH)2 (b≠6)的溶液,所得沉淀的物质的量不可能为
| A.5mol | B.3mol | C.b/2mol | D.5b/3mol |
查看答案和解析>>
科目:高中化学 来源:2012-2013学年河北省高三第三次模拟考试化学试卷(解析版) 题型:选择题
已知Ba(AlO2)2可溶于水,向含有1 mol Al2(SO4)3的溶液中加入含有b mol Ba(OH)2 (b≠6)的溶液,所得沉淀的物质的量不可能为
A.5mol B.3mol C.b/2mol D.5b/3mol
查看答案和解析>>
科目:高中化学 来源:2011-2012学年高三上学期化学一轮复习《从矿物到基础材料》专题综合测试(苏教版) 题型:选择题
已知Ba(AlO2)2可溶于水。右图表示的是向Al2(SO4)3溶液中逐滴加入Ba(OH)2溶液时,生成沉淀的物质的量y与加入Ba(OH)2的物质的量x的关系。
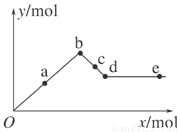
下列有关叙述正确的是( )
A.a~b时沉淀的物质的量:Al(OH)3比BaSO4多
B.c~d时溶液中离子的物质的量:Ba2+比AlO2-多
C.a~d时沉淀的物质的量:BaSO4可能小于Al(OH)3
D.d~e时溶液中离子的物质的量:Ba2+可能等于OH-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com