
【题目】下列关于硫的说法不正确的是
A. 试管内壁附着的硫可用二硫化碳溶解除去
B. 游离态的硫存在于火山喷口附近或地壳的岩层里
C. 单质硫既有氧化性,又有还原性
D. 硫在过量纯氧中的燃烧产物是三氧化硫
 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案 初中暑期衔接系列答案
初中暑期衔接系列答案科目:高中化学 来源: 题型:
【题目】某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是
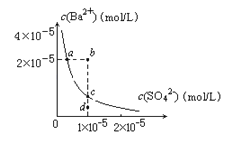
A. 加入Na2SO4可使溶液由a点变到b点
B. 通过蒸发可以使溶液由d点变到c点
C. d点无BaSO4沉淀生成
D. a点对应的Ksp大于c点对应的Ksp
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于金属氧化物的说法不正确的是( )
A.Fe3O4是具有磁性的黑色晶体
B.Al2O3能溶于酸和强碱,是两性氧化物
C.Na2O是碱性氧化物,可与H2O、CO2反应
D.FeO不稳定,在空气中受热迅速被氧化为Fe2O3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 测定HCl和NaOH中和反应的反应热时,单次实验均应测量3个温度,即盐酸起始温度、NaOH溶液起始温度和反应终止温度
B. 若2C(s) + O2(g) = 2CO(g) △H=—221.0kJ/mol,则碳的燃烧热为110.5 kJ/mol
C. 电解水可以获得H2和O2,该反应是放热反应
D. 已知I:反应H2(g)+Cl2(g)=2HCl(g) △H=-akJ/mol,II:![]() 且a、b、c均大于零,则断开1 mol H-Cl键所需的能量为2(a+b+c) kJ/mol
且a、b、c均大于零,则断开1 mol H-Cl键所需的能量为2(a+b+c) kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,相同的镁条与下列酸溶液反应,反应开始时放出H2最快的是( )
A.10mL 1mol/L 硫酸B.10mL 1mol/L 醋酸
C.10mL 3mol/L 硝酸D.40mL 1mol/L 盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂离子电池广泛用作便携式电源,其正极材料是决定锂离子电池可逆容量与循环寿命的关键因素之一。锂二次电池一般以LiCoO2、LiFePO4等为正极材料,以石墨碳为负极材料,以溶有LPF6、LiBF4等的碳酸二乙酯(DEC)为电解液。充电时,Li+从正极层状氧化物的晶格间脱出进入有机电解液,有机电解液中的Li+则进入负极,得电子后以原子形式嵌入到石墨材料的晶格中,即:6C+xLi++xe-=LixC6,如图所示:
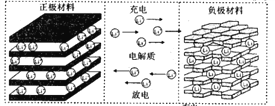
(1)如图所示,已知该电池电极总反应:LiCoO2+C![]() Li1-xCoO2+CLix,充电时,该电池的正极上的反应为_______________________。
Li1-xCoO2+CLix,充电时,该电池的正极上的反应为_______________________。
(2)放电时负极材料质量________(填“增加”、“减小”或“不变”)
(3)在实验室中,可用下列方案从废旧锂离子电池的正极材料中(主要含有LiCoO2、炭粉及少量Al、Fe等)回收钴和锂。

①溶解过程中,通入SO2时所发生反应的化学方程式为________________________;
②除杂过程中,所得沉淀的主要成分是___________________;(写化学式)
③常温下,已知Ksp[Co(OH)2]=1.09×10-15,若沉淀钴时pH=9.5,则溶液中Co2+是否沉淀完全?请列式计算说明。 _______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质的相互关系正确的是( )
A.同位素:H+、H2、2H、3H
B.同素异形体:C60、C70、C(石墨)
C.同分异构体:C3H8、C4H10
D.同系物:正丁烷、异丁烷
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com